- Grogan M et al. J Am Coll Cardiol 2016;68(10):1014–1020.
- McDonagh TA et al. Eur Heart J 2021;42(36):3599–3726.
- Maurer MS et al. N Engl J Med 2018;379(11):1007–1016.
- González-López E et al. Eur Heart J 2015;36(38):2585–2594.
- Maurer MS et al. Circulation 2017;135(14):1357–1377.
- Sekijima Y et al. Curr Pharm Des 2008;14(30):3219–3230.
- Vyndaqel® 61 mg, Fachinformation nach aktuellem Stand.
- Elliott P et al. Circ Heart Fail 2022;15(1):e008193.
- Lockwood PA et al. Clin Pharmacol Drug Dev 2020;9(7):849–854.
Kardiale Amyloidose als Ursache einer Herzinsuffizienz rechtzeitig erkennen und kausal behandeln
Einer chronischen Herzinsuffizienz können viele Ursachen zugrunde liegen – auch die häufig noch unterdiagnostizierte kardiale Amyloidose, die unbehandelt zu einer hohen Morbidität und Mortalität führt.<sup>1</sup> Die Prognose kann mit der leitliniengerechten Kausaltherapie deutlich verbessert werden.<sup>2,3</sup>
Hinter einer chronischen Herzinsuffizienz kann sich auch die infiltrative Systemerkrankung Transthyretin-Amyloidose mit Kardiomyopathie (ATTR-CM) verbergen, die als Ursache immer noch unterschätzt wird. Studien zeigen, dass bei bis zu 13,3 % der Patient:innen mit chronischer Herzinsuffizienz mit erhaltener Pumpfunktion (HFpEF) eine ATTR-CM nachgewiesen werden kann.4–6
Da die unbehandelte ATTR-CM aufgrund hoher Morbidität und Mortalität mit einer schlechten Prognose assoziiert ist, sind sowohl eine konsequente Diagnostik als auch eine zielgerichtete, kausale Behandlung ausschlaggebend.1
Passen die Befunde und Symptome nicht zu den Erwartungen einer bereits gestellten Diagnose? Dann sollte man in der hausärztlichen Praxis hellhörig werden – vor allem wenn vornehmlich männliche Patienten über 65 Jahre bei Verlaufskontrollen über eine Verschlechterung der Symptomatik (z. B. mangelnde Belastbarkeit, Dyspnoe, Ödeme in den Extremitäten) berichten – trotz adhärenter Herzinsuffizienz-Standardtherapie!
Bereits bei diesen ersten Indizien sollte umgehend eine kardiologische Praxis eingebunden werden. Dort können weitere bildgebende Diagnostikmaßnahmen (u. a. Echokardiografie) durchgeführt werden. Das Zusammenführen der unterschiedlichen klinischen Befunde ermöglicht eine frühzeitige Diagnose und Einleitung der Kausaltherapie.
Für Patient:innen mit ATTR-CM steht seit Februar 2020 mit dem Transthyretin-Stabilisator Tafamidis 61 mg (Vyndaqel® 61 mg) eine zielgerichtete Therapie der ATTR-CM zur Verfügung.7 Die Zulassung basiert auf den Daten der multizentrischen, doppelblinden, randomisierten, placebokontrollierten Phase-3-Studie ATTR-ACT (Transthyretin Amyloidosis Cardiomyopathy Clinical Trial) mit 441 Patient:innen über 30 Monate aus 48 Studienzentren in 13 Ländern.3
Die ATTR-ACT-Studie untersuchte die Wirksamkeit und Sicherheit von Tafamidis bei ATTR-CM.*,3,7,8
- ⮚ Die Studie zeigte über einen Zeitraum von 30 Monaten
- eine signifikante Senkung der Gesamtmortalität um 30 % (p = 0,0259)3
- eine signifikante Reduktion kardiovaskulär bedingter Hospitalisierungen um 32 % (p < 0,0001)3
- ⮚ Darüber hinaus zeigten sich bereits nach 6 Monaten signifikante Vorteile für Patient:innen unter Tafamidis hinsichtlich
- Lebensqualität (Kansas-City-Kardiomyopathie-Fragebogen, KCCQ; p < 0,001)3
- Leistungsfähigkeit (6-Minuten-Gehtest, 6-MWT; p < 0,001)3
- ⮚ Das Sicherheitsprofil von Tafamidis war mit dem von Placebo vergleichbar.3
- ⮚ Die Langzeitwirksamkeit von Tafamidis wurde neben der ATTR-ACT-Studie in deren Verlängerungsstudie bestätigt.8
Auch die aktuelle Leitlinie der Europäischen Gesellschaft für Kardiologie (ESC) empfiehlt aufgrund dieser positiven Daten Tafamidis bei Patient:innen mit ATTR-CM mit dem höchsten Empfehlungsgrad I.2
Die Studienergebnisse und Leitlinienempfehlungen belegen, dass eine frühe Diagnose und kausale Behandlung bei ATTR-CM von großer Bedeutung sind. Die Behandlung erfolgt in der Regel in Amyloidose-Zentren oder in kardiologischen Praxen, die sich auf die Diagnose und Therapie von Patient:innen mit ATTR-CM spezialisiert haben.
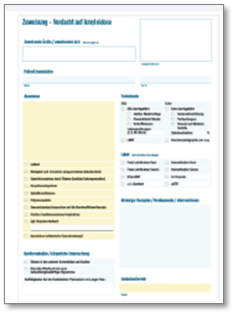
Nutzen Sie deshalb diesen Zuweiserbogen, der Sie in Ihrem Praxisalltag bei der Dokumentation der Anamnese, der körperlichen Untersuchungen oder bei Auffälligkeiten im EKG Ihrer Herzinsuffizienz-Patient:innen unterstützt. Denken Sie bereits in Ihrer hausärztlichen Praxis daran: Je früher die umfassenden Befunde zusammengeführt werden und je früher die interdisziplinäre Zusammenarbeit mit der kardiologischen Praxis initiiert wird, desto früher kann auch die gesicherte Diagnose ATTR-CM gestellt werden und die leitliniengerechte, krankheitsmodifizierende Kausaltherapie mit Vyndaqel® (Tafamidis) 61 mg eingeleitet werden.2,3,7
* In der Studie wurden Tafamidis-Meglumin 80 mg und 20 mg untersucht. Die zugelassene Formulierung mit 61 mg Tafamidis entspricht 80 mg Tafamidis-Meglumin. Damit Patient:innen nicht vier 20-mg-Tafamidis-Meglumin-Weichkapseln täglich einnehmen müssen, hat Pfizer die Weichkapsel mit 61 mg Tafamidis als freie Säure entwickelt. Die Bioäquivalenzstudie zeigte, dass die relative Bioverfügbarkeit von 61 mg Tafamidis ähnlich wie bei 80 mg Tafamidis-Meglumin nach wiederholter oraler Einnahme ist.9