Die Bedeutung kardiovaskulärer Komorbiditäten in der CLL-Therapie
Komorbide Patienten mit chronischer lymphatischer Leukämie sollten bevorzugt eine Therapie mit gutem Sicherheits- und Verträglichkeitsprofilerhalten. Dabei spielen kardiovaskuläre Aspekte eine besondere Rolle – mit Blick auf Komorbiditäten und Unterschiede im Nebenwirkungsprofil der verfügbaren Therapeutika.
Dank der kontinuierlichen Weiterentwicklung von Therapieoptionen, sind die Überlebenschancen von Patienten mit chronischer lymphatischer Leukämie (CLL) im Laufe der Zeit deutlich gestiegen. Die relative 5-Jahres-Überlebensrate, liegt für CLL-Patienten mittlerweile bei über 82 %1. Bei der CLL handelt es sich in der Regel um eine Erkrankung älterer Menschen. Etwa 90 % der Patienten sind zum Zeitpunkt der Diagnosestellung mindestens 55 Jahre2 alt, das mediane Erkrankungsalter liegt in Deutschland bei 72 bzw. 75 Jahren (Männer bzw. Frauen)1.
Zweidrittel der CLL-Patienten haben kardiovaskuläre Komorbiditäten
Mit dem fortgeschrittenen Patientenalter geht ein hohes Maß an Begleiterkrankungen einher. So wiesen in einer prospektiven Kohortenstudie 93 %3 von über 1.100 CLL-Patienten bei Diagnosestellung mindestens eine und im Median drei Komorbiditäten auf. In mehr als Zweidrittel der Fälle handelte es sich um ein kardiovaskuläres Leiden.3
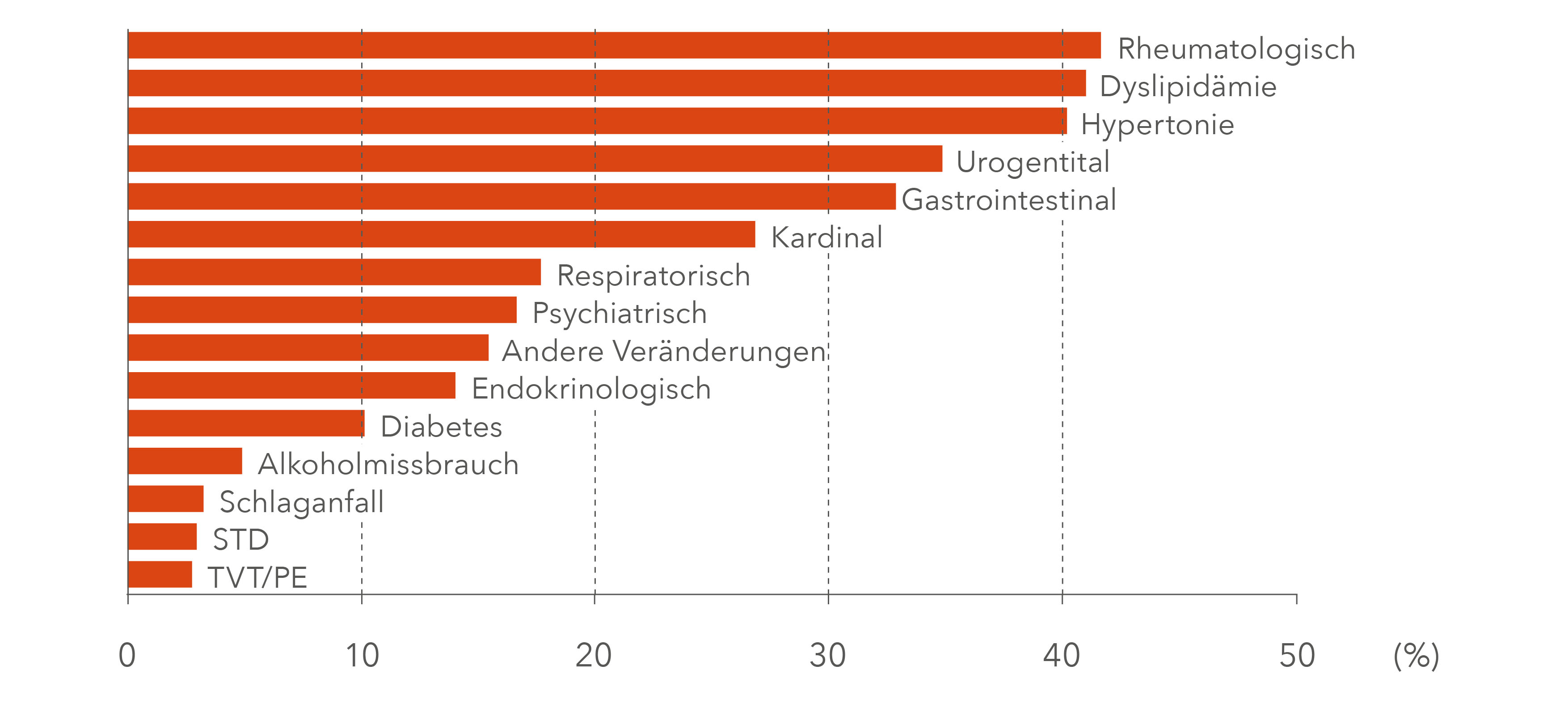 Komorbiditäten zu Beginn einer prospektiven Kohortenstudie mit 1.143 neu diagnostizierten CLL-Patienten (adaptiert nach Strati et al 20173).
Komorbiditäten zu Beginn einer prospektiven Kohortenstudie mit 1.143 neu diagnostizierten CLL-Patienten (adaptiert nach Strati et al 20173).
Komorbiditäten haben einen signifikant negativen Einfluss auf das Therapieergebnis bei CLL-Patienten.4 Bei Organfehlfunktion und schlechtem Allgemeinzustand sind gut tolerierbare Therapien notwendig.3,5 In der Praxis spielt damit die sorgfältige Ermittlung des Komorbiditätsstatus für die Auswahl des am besten geeigneten Therapieansatzes und als prädiktiver Faktor eine wichtige Rolle. Im Studien-Setting hat die Dokumentation und Stratifizierung auf der Basis von Komorbiditäten-Scores an Bedeutung gewonnen.4
Aktualisierte Onkopedia-Leitlinie präferiert BTKi bei komorbiden Patienten
Auch in der aktuellen Onkopedia-Leitlinie zur CLL richtet sich die Wahl der Arzneimittel neben anderen Faktoren nach dem Allgemeinzustand und der Komorbidität des Patienten, ermittelt z.B. durch den CIRS-Score.1 Die Autoren der im September 2020 aktualisierten Leitlinienversion heben zusammenfassend hervor, dass „komorbide Patienten präferentiell eine Primärtherapie mit einem BTK-Inhibitor“ erhalten sollten. Alternativ zum Einsatz der Bruton-Tyrosinkinase-Inhibitoren (BTKi) mit oder ohne Anti-CD20-Antikörper kommt eine Primärtherapie mit dem BCL-2-Inhibitor Venetoclax plus Obinutuzumab in Betracht. Die Chemoimmuntherapie verliert zunehmend an Bedeutung und wird nur noch bei Patienten ohne genetische Risikofaktoren als leitliniengerechte Option betrachtet.1
Insgesamt werden in der Leitlinie die zielgerichteten Ansätze BTKi ± Anti-CD20-AK und Venetoclax + Obinutuzumab in der Erstlinie sowie BTKi als Monotherapie und Venetoclax + Rituximab in der Zweitlinie – dort u.a. abhängig von der jeweiligen Vorbehandlung – für jede Patientenpopulation empfohlen, unabhängig von Risikofaktoren, Alter und reduziertem Allgemeinzustand.1
BTKi der ersten Generation: Kardiotoxizität wirkt therapielimitierend
Für das therapeutische Management der CLL, bei der häufig eine Langzeittherapie erforderlich werden kann, resultiert aus einer hohen Komorbiditätslast der Patienten ein erhöhter Bedarf an Medikamenten mit guter Verträglichkeit und möglichst geringer Toxizität – gerade im Hinblick auf das kardiovaskuläre Risiko.
BTKi der ersten Generation sind zwar gut wirksam, im realen Versorgungsalltag bricht allerdings ein relevanter Teil der Patienten (bis zu 23 %5) eine Ibrutinib-Therapie aufgrund von Unverträglichkeiten vorzeitig ab.Dabei wird neben dem Auftreten von schweren Blutungen eine Ibrutinib-assoziierte Kardiotoxizität beobachtet.8 In einer retrospektiven Kohortenstudie stellte sich das Auftreten von Vorhofflimmern (VHF) als häufigster Grund für ein vorzeitiges Therapieende unter Ibrutinib heraus.9 Eine Metaanalyse ermittelte beim Einsatz des Erstgenerations-BTKi eine vierfach erhöhte VHF-Inzidenz gegenüber anderen Therapien.10 Auch über plötzlichen Herztod und ventrikuläre Arrhythmien kurz nach Therapiestart mit Ibrutinib wurde berichtet.11 Zum bekannten Nebenwirkungsprofil von Ibrutinib zählt auch die Entwicklung oder Verschlechterung einen Hypertonus. Dies ist mit einem zweifach erhöhten Risiko für weitere kardiale Ereignisse assoziiert.12
Hochselektiver BTKi der zweiten Generation: überzeugendes Sicherheitsprofil
Hier ergeben sich nun neue Perspektiven durch die Verfügbarkeit von Acalabrutinib (Calquence®). Der hochselektive BTKi wurde schon vor seiner EU-Zulassung im November 2020 in die Onkopedia-Leitlinie aufgenommen und erweitert das BTKi-Spektrum als zweiter Vertreter der Substanzklasse neben Ibrutinib.1,13
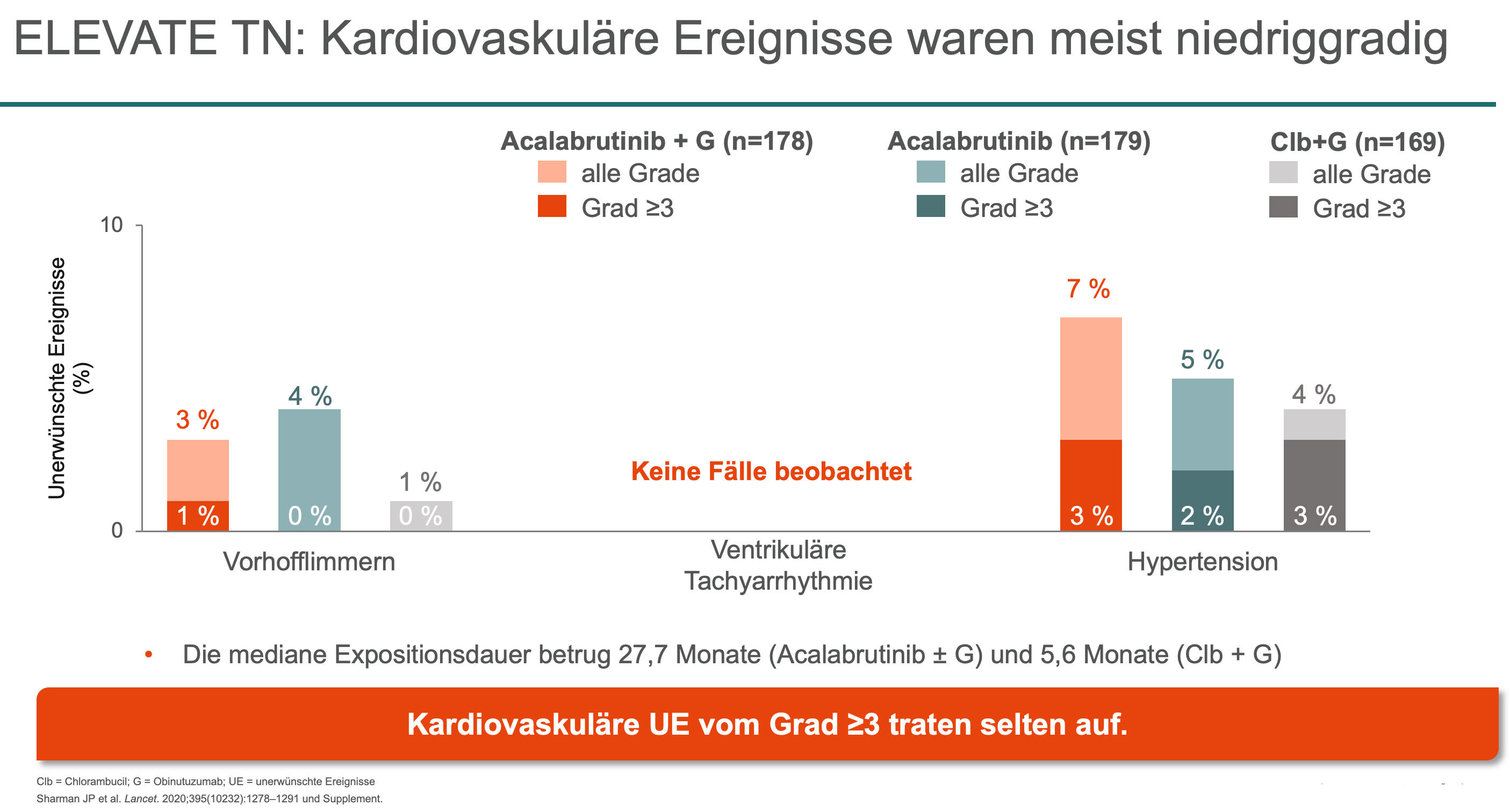
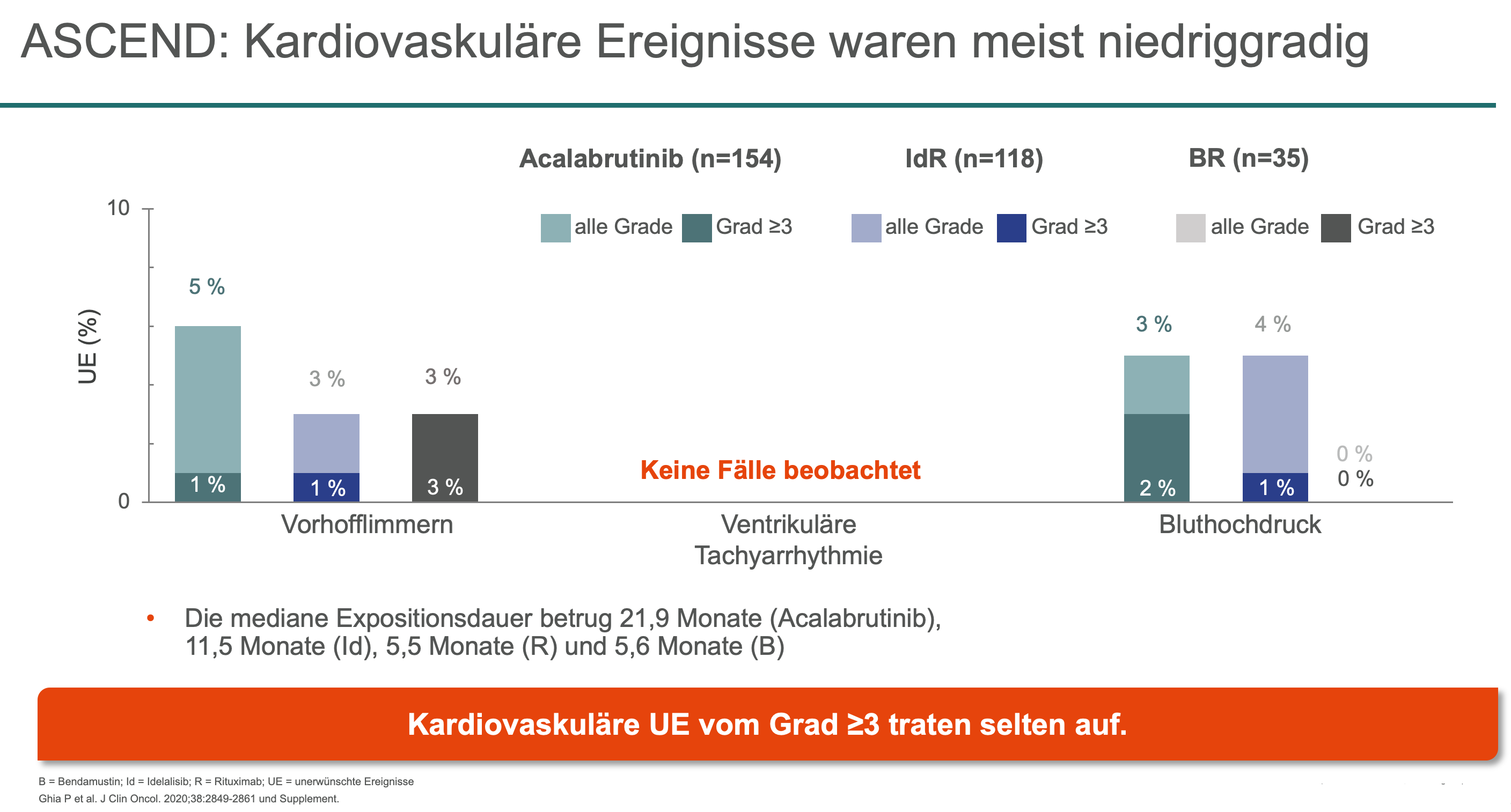
Hinter der Entwicklung von Acalabrutinib als BTKi der zweiten Generation steht die Überlegung, durch eine höhere Selektivität die Off-Target-Effekte zu minimieren und deren mögliche Auswirkungen auf das Nebenwirkungsprofil günstig zu beeinflussen. In den Zulassungsstudien ELEVATE TN14 und ASCEND15 wurde für Acalabrutinib neben der starken Wirksamkeit (24-Monats-PFS-Rate mit Alacalabrutinib plus Obinutuzumab: 93 %) auch ein günstiges Verträglichkeits- und Sicherheitsprofil belegt, mit einer Rate an kardialen Ereignissen, die in der Größenordnung mit der im Kontrollarm vergleichbar ist. Zu berücksichtigen ist hier die viel längere Expositionsdauer in den Acalabrutinib-Armen.
Aktuelle Publikationen bestätigen Vorteile unter kardiovaskulärem Aspekt
Wie sich in den Zulassungsstudien zeigte, können Patienten über alle Subgruppen hinweg von der Behandlung mit Acalabrutinib profitieren.14,15 Zwei bei der ASH-Tagung 2020 präsentierte Metaanalysen16,17 bestätigen die günstigen Eigenschaften des Zweitgenerations-BTKi hinsichtlich der kardiovaskulären Nebenwirkungen. Kardiale Ereignisse führten nur in 0,9 %17 der Fälle zu einem Therapieabbruch. Die Inzidenz von Vorhofflimmern unter Acalabrutinib entsprach mit 4 %17 in etwa derjenigen in der allgemeinen CLL-Population.
Eine aktuelle kanadische Publikation spricht sich angesichts des überzeugenden kardialen Sicherheitsprofils für den breiten Einsatz von Acalabrutinib aus.18
Positive Tendenz im direkten BTKi-Vergleich
Mit Spannung werden die Ergebnisse aus dem direkten BTKi-Vergleich in der noch laufenden Phase-III-Studie ELEVATE RR19 erwartet. Hier zeichnen sich bereits positive Tendenzen zugunsten des BTKi der zweiten Generation ab: Zu Jahresbeginn 2021 wurde – neben der Nichtunterlegenheit hinsichtlich des progressionsfreien Überlebens als dem primären Studienendpunkt – über eine signifikant geringere Rate an Vorhofflimmern (sekundärer Endpunkt) unter Acalabrutinib gegenüber Ibrutinib bei vorbehandelten Patienten mit Hochrisiko-CLL berichtet.20
- Wendtner CM et al. Onkopedia-Leitlinie Chronische Lymphatische Leukämie (CLL). Stand: September 2020. https://www.onkopedia.com/de/onkopedia/guidelines/chronische-lymphatische-leukaemie-cll/@@guideline/html/index.html
- Eichhorst B et al. Chronic lymphocytic leukaemia: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2015;26(suppl 5):v78-v84
- Strati P et al. Relationship between co-morbidities at diagnosis, survival and ultimate cause of death in patients with chronic lymphocytic leukaemia (CLL): a prospective cohort study. Br J Haematol 2017;178(3):394-402
- Goede V et al. Interactions between comorbidity and treatment of chronic lymphocytic leukemia: results of German Chronic Lymphocytic Leukemia Study Group trials. Haematologica 2014;99(6):1095-100
- Sharman JP et al. Understanding Ibrutinib Treatment Discontinuation Patterns for Chronic Lymphocytic Leukemia. Blood 2017;130:4060 (ASH Abstr)
- Mato AR et al. Toxicities and outcomes of 616 ibrutinib-treated patients in the United States: a real-world analysis. Haematologica 2018;103(5):874-9
- Hampel PJ et al. Rapid disease progression following discontinuation of ibrutinib in patients with chronic lymphocytic leukemia treated in routine clinical practice. Leuk Lymphoma 2019;60(11):2712-9
- More L et al. Ibrutinib-Associated Cardiotoxicity. https://www.acc.org/latest-in-cardiology/articles/2020/01/21/08/46/ibrutinib-associated-cardiotoxicity (Zugriff am 15.03.2021)
- Mato AR et al. Outcomes of CLL patients treated with sequential kinase inhibitor therapy: a real world experience. Blood 2016;128:2199-205
- Leong DP et al. The risk of atrial fibrillation with ibrutinib use: a systematic review and meta-analysis. Blood 2016;128:138-40
- Lampson BL et al. Ventricular arrhythmias and sudden death in patients taking ibrutinib. Blood 2017;129:2581-4
- Dickerson T et al. Hypertension and incident cardiovascular events following ibrutinib initiation. Blood 2019;134:1919-28.
- Fachinformation Calquence®, Stand November 2020
- Sharman JP et al. Acalabrutinib with or without obinutuzumab versus chlorambucil and obinutuzumab for treatment-naive chronic lymphocytic leukaemia (ELEVATE TN): a randomised, controlled, phase 3trial. Lancet 2020;395:1278-91
- Ghia P et al. ASCEND: Phase III, Randomized Trial of Acalabrutinib Versus Idelalisib Plus Rituximab or Bendamustine Plus Rituximab in Relapsed or Refractory Chronic Lymphocytic Leukemia. J Clin Oncol 2020;38(25):2849-61
- Hilal T et al. Adverse Events in Clinical Trials of Ibrutinib and Acalabrutinib for B-Cell Lymphoproliferative Disorders: A Systematic Review and Network Meta-Analysis. ASH 2020, Abstract 1317
- Brown JR et al. Pooled Analysis of Cardiovascular Events from Clinical Trials Evaluating Acalabrutinib Monotherapy in Patients with Chronic Lymphocytic Leukemia (CLL). ASH 2020, Abstract 3146
- Banerji V et al. Bruton tyrosine kinase inhibitors for the frontline treatment of chronic lymphocytic leukemia. Curr Oncol 2020;27(6): e645-55
- Study of Acalabrutinib (ACP-196) Versus Ibrutinib in Previously Treated Subjects With High Risk CLL. ClinicalTrials.gov Identifier: NCT02477696. https://clinicaltrials.gov/ct2/show/NCT02477696
- Calquence met primary efficacy endpoint in head-to-head trial against ibrutinib in chronic lymphocytic leukaemia. News release. AstraZeneca. Published January 25, 2021
Abkürzungen:
BCL-2 = B-Zell-Lymphom-2- (Protein)
BTK = Bruton-Tyrosinkinase
BTKi = Bruton-Tyrosinkinase-Inhibitor
CIRS = Cumulative Illness Rating Scale
CLL = chronische lymphatische Leukämie
DE-34560\21


