Acalabrutinib auch bei Hochrisiko-Patient:innen langanhaltend wirksam
Bestimmte genetische Veränderungen können die Prognose bei Patient:innen mit chronischer lymphatischer Leukämie (CLL) deutlich verschlechtern. Umso wichtiger sind wirksame Therapiestrategien bei genau diesen Risikopersonen.
Kernpunkte:
- Bei etwa 1 von 2 CLL-Patient:innen liegt mindestens ein intermediäres genetisches Risikoprofil vor.1-4
- Der Bruton-Tyrosinkinase-Inhibitor (BTKi) Acalabrutinib zeigt unabhängig von genetischen Risikofaktoren eine hohe, langanhaltende Wirksamkeit.5
- Acalabrutinib +/- Obinutuzumab erzielt gegenüber der Standard-Chemoimmuntherapie bei Risikopatient:innen signifikant höhere PFS-Raten.5
Therapie je nach genetischem Risikoprofil
Der Mutationsstatus der vorliegenden CLL dient nicht nur der formalen Einordnung und Klassifizierung, sondern ist auch prognostisch entscheidend und bestimmt über die Wahl der Therapie. Eine genetische Untersuchung auf relevante Mutationen wird daher vor Beginn der Behandlung empfohlen.6
Als genetische Risikofaktoren bei der CLL gelten:6
- Deletion del(17p) bzw. TP53-Mutation
- komplexer Karyotyp (3 und mehr Aberrationen)
- IGHV-Status unmutiert (IGHVunmut)
Entsprechend richtet sich das Therapieschema nach folgenden genetischen Risikogruppen:6
- keine del(17p13)/TP53-Mutation, kein komplexer Karyotyp-Status, IGHV mutiert
- keine del(17p13)/TP53-Mutation, kein komplexer Karyotyp-Status, IGHV unmutiert
- del(17p13)/TP53-Mutation und/oder komplexer Karyotyp-Status, unabhängig vom IGHV-Status
Acalabrutinib: hohe PFS-Raten auch bei Risikogruppen
In der Phase-III-Studie ELEVATE-TN mit therapienaiven CLL-Patient:innen wurden diese unterschiedlichen genetischen Risikogruppen in einer Supgruppenanalyse näher untersucht.7 Verglichen wurde die Wirksamkeit des BTK-Inhibitors Acalabrutinib (Calquence®) – als Monotherapie oder in Kombination mit dem CD20-Antikörper Obinutuzumab (G) – mit der Standard-Chemoimmuntherapie aus Chlorambucil (Clb) und Obinutuzumab (G). Die neuesten 6-Jahres-Daten dieser Studie zeigen: Die zielgerichtete Behandlung mit dem Zweitgenerations-BTKi Acalabrutinib wirkt auch unabhängig von genetischen Risikofaktoren zuverlässig und nachhaltig.5
Die Subgruppe mit unmutiertem IGHV-Status erreichte unter Acalabrutinib + G nach 72 Monaten eine geschätzte PFS-Rate (progressionsfreies Überleben) von bis zu 75 %. Im Vergleich zur Standard-Chemoimmuntherapie bedeutet das eine signifikante Risikoreduktion um bis zu 92 % (HR (95 %-KI): 0,08 (0,05–0,12), p < 0,0001).5
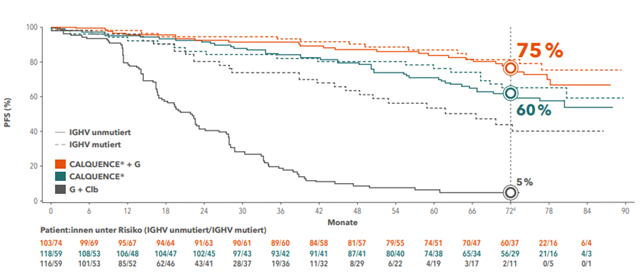
Abb. 1: PFS-Raten in Abhängigkeit des IGHV-Status. Adaptiert nach Sharman JP et al. 2023.5
Auch bei Patient:innen mit einer prognostisch ungünstigen Deletion del(17p) und/oder einer TP53-Mutation blieb die Wirksamkeit von Acalabrutinib über die Jahre bestehen. Sowohl in der Kombination mit Obinutuzumab als auch bei der Monotherapie betrugen die geschätzten PFS-Raten 56 %, während unter Clb + G lediglich 18 % erreicht wurden.5 Dies entsprach einer Risikoreduktion von 77 % für die Monotherapie (HR (95 %-KI): 0,23 (0,10–0,52), p = 0,0002) bzw. 72 % für die Kombinationsbehandlung (HR (95 %-KI): 0,28 (0,13–0,59), p = 0,0009) gegenüber der Chemoimmuntherapie.5
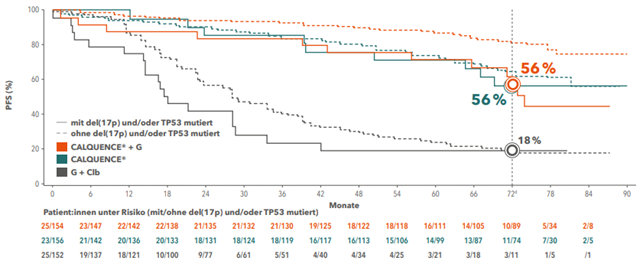
Abb. 2: PFS-Raten in Abhängigkeit von del(17p) und/oder TP53-Mutation. Adaptiert nach Sharman JP et al. 2023.5
Klare Leitlinien-Empfehlung: BTKi vor CIT und SZT
Wie viele Betroffene von diesen Ergebnissen profitieren können, zeigen folgende Zahlen: So weist mehr als die Hälfte der rund 5000 Patient:innen, die jedes Jahr an chronischer lymphatischer Leukämie erkranken, einen unmutierten IGHV-Status und damit nach Leitlinie ein intermediäres Risiko auf.1,2,6,8 Zum genetischen Hochrisiko-Kollektiv gehören immerhin bis zu einem Drittel der Erkrankten.3,4,6
Nach aktueller Leitlinien-Empfehlung sind BTKi der zweiten Generation wie Acalabrutinib und Zanubrutinib bei diesen Patient:innen erste Wahl.6 Mit der effektiven molekularen Behandlung rückt auch der Stellenwert von Chemotherapie und allogener Stammzelltransplantation (alloSZT) bei der CLL weiter in den Hintergrund.
- Delgado J et al. Chronic lymphocytic leukemia: A prognostic model comprising only two biomarkers (IGHV mutational status and FISH cytogenetics) separates patients with different outcome and simplifies the CLL-IPI. Am J Hematol. 2017;92:375–380.
- International CLL-IPI Working Group. An international prognostic index for patients with chronic lymphocytic leukaemia (CLL-IPI): a meta-analysis of individual patient data. Lancet Oncol. 2016;17:779–790 (und Supplement).
- Campo E et al. TP53 aberrations in chronic lymphocytic leukemia: an overview of the clinical implications of improved diagnostics. Haematologica. 2018;103:1956–1968.
- Ghia P et al. ASCEND: Phase III, Randomized Trial of Acalabrutinib Versus Idelalisib Plus Rituximab or Bendamustine Plus Rituximab in Relapsed or Refractory Chronic Lymphocytic Leukemia. J Clin Oncol. 2020;38:2849–2861.
- Sharman JP et al. Acalabrutinib ± Obinutuzumab Vs Obinutuzumab + Chlorambucil in Treatment-Naive Chronic Lymphocytic Leukemia: 6-Year Follow-up of Elevate-TN. Präsentiert auf: American Society of Hematology (ASH) Annual Meeting; 9.–12. Dezember 2023, San Diego, California.
- Wendtner CM et al. Onkopedia-Leitlinie. Chronische Lymphatische Leukämie (CLL). Stand: Januar 2023. Online verfügbar unter: https://www.onkopedia.com/de/onkopedia/guidelines/chronische-lymphatische-leukaemie-cll/@@guideline/html/index.html (letzter Aufruf: Februar 2024).
- Sharman JP et al. Acalabrutinib with or without obinutuzumab versus chlorambucil and obinutuzumab for treatment-naive chronic lymphocytic leukaemia (ELEVATE-TN): a randomised, controlled, phase 3 trial. Lancet. 2020;395:1278–1291.
- Zentrum für Krebsregisterdaten: Leukämien. Online verfügbar unter: https://www.krebsdaten.de/Krebs/DE/Content/Krebsarten/Leukaemien/leukaemien_node.html (letzter Aufruf: Februar 2024).
Abkürzungen:
BTK = Bruton-Tyrosinkinase
CLL = Chronische lymphatische Leukämie
HR = Hazard ratio
KI = Konfidenzintervall
PFS = Progressionsfreies Überleben
SZT= Stammzelltransplantation

