Therapie der CLL: Generationswechsel bei den BTK-Inhibitoren
In den vergangenen Jahren haben sich die therapeutischen Optionen bei der CLL rasant weiterentwickelt. Nach Erscheinen der letzten Leitlinienversion im September 2020 hat sich mit Acalabrutinib die zweite Generation von Bruton-Tyrosinkinase-Inhibitoren in der Therapie der CLL etabliert. Jetzt ziehen die Empfehlungen nach und rücken die neuen BTKi an erste Stelle.
Kernpunkte: Was ist neu?
- BTKi der zweiten Generation sind sowohl in der Erstlinien- als auch in der Zweitlinientherapie aufgrund ihres reduzierten Toxizitätsprofils gegenüber der ersten Generation zu bevorzugen.
- Der Stellenwert der Chemotherapie rückt in den Hintergrund.
- Bei der Erstlinientherapie entfallen Alter und Fitness als Stratifizierungsparameter.
Eine Erfolgsgeschichte
Seit den Anfängen mit Chlorambucil hat sich in der Behandlung der chronischen lymphatischen Leukämie viel getan. Die Errungenschaften der Forschung haben im Lauf der Jahre zahlreiche neue Substanzen hervorgebracht. Immer präziser wurden deren Angriffspunkte, immer selektiver ihr Bindungsverhalten. Das hat in den letzten Dekaden zu handfesten Erfolgen bei der CLL-Therapie geführt. Lag die 5-Jahres-Überlebensrate in den 70er Jahren noch bei etwa 65 %, stieg sie bis zum Jahr 2021 auf gut 87 %.1
Derzeitiger Höhepunkt dieser Entwicklung ist die Etablierung hochselektiver Inhibitoren der Bruton-Tyrosinkinase (BTK). Der antineoplastische Effekt dieser Wirkstoffe beruht auf der Hemmung dieser zentralen Schaltstelle in der Signaltransduktion von B-Lymphozyten. Indem sie an das aktive Zentrum der BTK binden, hemmen sie deren enzymatische Aktivität nachhaltig und verhindern so die weitere Proliferation der entarteten Zellen.2
Mit Acalabrutinib (Calquence®) steht seit November 2020 die zweite Generation der BTKi zur Verfügung, die insbesondere durch ihre bessere Verträglichkeit einen erheblichen Vorteil im Therapiemanagement der CLL bringt.
Erstlinientherapie im Überblick
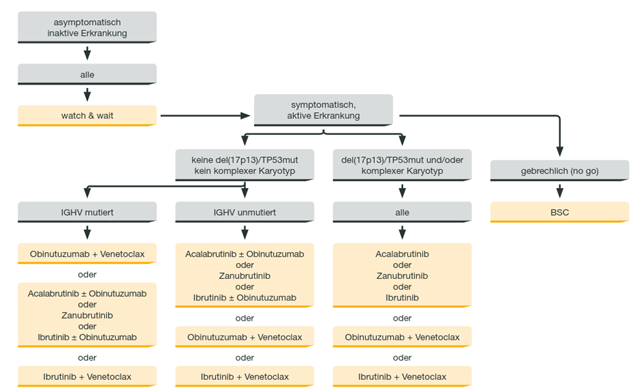 Abbildung 1: Erstlinientherapie der CLL. Adaptiert nach: Onkopedia-Leitlinie CLL. Stand: Januar 2023, letzter Zugriff: Mai 2023.3
Abbildung 1: Erstlinientherapie der CLL. Adaptiert nach: Onkopedia-Leitlinie CLL. Stand: Januar 2023, letzter Zugriff: Mai 2023.3
Bei der primären Behandlung stehen verschiedene Therapieoptionen zur Verfügung. Dabei fällt schon auf den ersten Blick auf: Alter und Allgemeinzustand dienen in der neuen Leitlinie nicht mehr als Stratifizierungsparameter. Stattdessen sollte sich die Therapiewahl primär an Komborbiditäten sowie am molekularen und zytogenetischen Status orientieren.
Therapiewahl abhängig vom genetischen Risiko
Als Erstlinientherapie ist grundsätzlich eine dauerhafte oder eine zeitlich begrenzte Behandlung möglich. Welcher Therapieoption der Vorzug gegeben werden soll, lässt sich noch nicht abschließend beurteilen. Die Leitlinienautoren geben derzeit bei niedrigem Risiko (mutierter IGVH-Status, keine TP53-Mutation, kein komplexer Karyotyp) dem BCL2-Inhibitor den Vorrang, während sie bei einem intermediären Risiko (unmutierter statt mutierter IGVH-Status) primär für einen Zweitgenerations-BTK-Inhibitor plädieren.3 Auch bei einem hohen genetischen Risiko (TP53-Mutation, komplexer Karyotyp) sind BTKi (bevorzugt der zweiten Generation) nach Expertenmeinung eher die erste Wahl.3
Acalabrutinib punktet mit Komfort und Sicherheit
Ein nicht zu unterschätzender Vorteil der neuen BTKi gegenüber der Kombination Venetoclax/Obinutuzumab (VenO) liegt in der vollständig oralen Applikation – für viele Patientinnen und Patienten ein klarer Pluspunkt, da sie das Medikament bequem zuhause oder unterwegs einnehmen können und nicht auf die Infusion in Praxis oder Klinik angewiesen sind. Bei Acalabrutinib verspricht die neue Tablettenform anstelle der Hartkapseln künftig weiteren Komfort.
Die ausdrückliche Präferenz der zweiten Generation der BTKi bei einem intermediären bis hohen genetischen Risiko ist ein wichtiges Novum gegenüber der letzten Leitlinienversion. Hintergrund ist das günstigere Toxizitätsprofil von Acalabrutinib im Vergleich zu seinem Vorgänger Ibrutinib, wie bereits 2020 in einer Metaanalyse deutlich wurde.4 In der Rezidivstudie ELEVATE-RR zeigte sich im direkten Head-to-Head-Vergleich mit Ibrutinib ein signifikant reduziertes Risiko für Arrhythmien und hypertensive Ereignisse – und das bei gleicher Wirksamkeit.5 Auch Harnwegsinfekte, Arthralgien und Diarrhoen waren seltener unter der Nachfolgegeneration. Die bessere Verträglichkeit machte sich wiederum im Behandlungsmanagement bemerkbar und führte zu weniger Therapieabbrüchen.5
Klarer Vorteil bei kardiologischen Komorbiditäten
In einem Kommentar zu ELEVATE-RR äußerte sich Prof. Dr. Erhard Hiller, Medizinisches Zentrum für Hämatologie und Onkologie München MVZ GmbH, hinsichtlich der praktischen Relevanz: „Vor die Wahl gestellt, würde ich mich schon wegen des geringeren Risikos der Nebenwirkung Vorhofflimmern und des erhöhten Risikos, die Substanz vorzeitig wieder absetzen zu müssen, für das Acalabrutinib entscheiden. Dies sollte wahrscheinlich auch für CLL-Patienten mit bekannten kardiologischen Vorerkrankungen gelten.“6
Die Leitlinienautoren sehen das offenbar ähnlich. Die Ergebnisse der Rezidivstudie lassen sich nach ihrer Ansicht im Analogieschluss auch auf die Erstlinientherapie übertragen. Die Empfehlung fällt daher bei einer Therapieinitiierung klar zugunsten der neuen BTKi aus.
Auch in der klinischen Praxis hat sich der neue Wirkstoff Acalabrutinib seit seiner Zulassung für die CLL Ende 2020 gegenüber seinem Vorgänger Ibrutinib bewährt. In einem Review mit mehreren Case Reports wurden jüngst die Vorteile von Acalabrutinib im Management der CLL herausgestellt.7
Zweitlinientherapie im Überblick
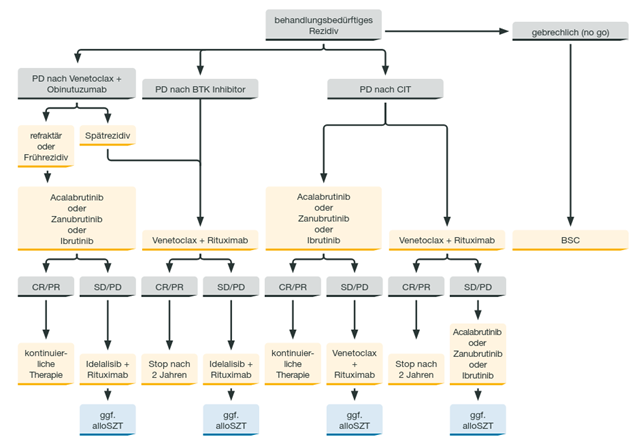 Abbildung 2: Therapie der CLL bei Rezidiv und Refraktärität. Adaptiert nach: Onkopedia-Leitlinie CLL. Stand: Januar 2023, letzter Zugriff: Mai 2023.3
Abbildung 2: Therapie der CLL bei Rezidiv und Refraktärität. Adaptiert nach: Onkopedia-Leitlinie CLL. Stand: Januar 2023, letzter Zugriff: Mai 2023.3
Neue BTKi auch in zweiter Linie erste Wahl
In der Zweitlinientherapie richtet sich die Wahl der Substanzen hauptsächlich nach der jeweiligen Vorbehandlung. Daneben spielen auch Alter, Komorbiditäten, die erreichte Remissionsdauer und mögliche Resistenzen eine Rolle. Nach einer Chemoimmuntherapie besteht wahlweise die Option für BTKi oder Venetoclax, hier mit dem Kombinationspartner Rituximab, einem anderen Anti-CD20-Antikörper. Nach Erstlinienbehandlung mit einer der beiden zielgerichteten Regime kommt die jeweils andere Wirkstoffklasse zum Zug. Bei einem Spätrezidiv (Remissionsdauer länger als 2-3 Jahre) nach zeitlich begrenzter Therapie kann die Primärbehandlung auch wiederholt werden.
Auch in der Rezidivtherapie ist die neue BTKi-Generation angekommen. Acalabrutinib und Zanubrutinib sind erste Wahl, Ibrutinib gilt nur als Ausweichtherapie bei Kontraindikationen oder Nicht-Verfügbarkeit der Nachfolger.
Chemotherapie ist out
Was hat sich ansonsten noch geändert? Klar ist: Die klassische Chemoimmuntherapie hat bei der CLL nahezu ausgedient. Das hat zuletzt die vierarmige Vergleichsstudie CLL13 gezeigt, bei der die Standard-Chemoimmuntherapie mit verschiedenen zielgerichteten Behandlungsschemata verglichen wurde.8 Prof. Dr. Clemens-Martin Wendtner, Chefarzt der Klinik für Hämatologie, Onkologie, Immunologie, Palliativmedizin, Infektiologie und Tropenmedizin der München Klinik Schwabing und Hauptautor der neuen Leitlinie, kündigte bereits beim EHA-Kongress 2022 an: „Um es griffig zusammenzufassen: CLL13 ist letztlich der Sargnagel für die Chemoimmuntherapie bei der CLL.“9
So beschränkt sich die klassische Behandlung mit Chlorambucil/Obinutuzumab bzw. Bendamustin/Rituximab aktuell auf Patientinnen und Patienten, die eine Therapie mit einem Signalwegsinhibitor ablehnen oder aufgrund von schweren Komorbiditäten nicht dafür geeignet sind.
Als ultima ratio hat auch die allogene Stammzelltransplantation nach wie vor ihren Platz im Therapieschema der CLL. Allerdings ist ihr Stellenwert in der Rezidivbehandlung durch die modernen Therapiemöglichkeiten in den Hintergrund gerückt. Sie ist lediglich bei ungünstiger Prognose und Wirkungsverlust von BTKi und Venetoclax zu erwägen.
Leitlinie in stetigem Fluss
In ihren aktuellen Empfehlungen greift die Leitlinienkommission die neuesten Daten aus Forschung und Praxis auf. Mit seinem günstigen Nebenwirkungsprofil hat sich Acalabrutinib gegenüber Ibrutinib nun auch formal durchgesetzt.
Seit der letzten Aktualisierung der Onkopedia-Leitlinie sind gut zwei Jahre vergangen. Wie lange die derzeitige Version aktuell bleibt, wird die weitere Dynamik in der Therapielandschaft der CLL zeigen.

DE-58051/23
Ausblick: EHA 2023 vom 8.-15. Juni in Frankfurt a. Main
Mit einem vielfältigen Programm lockt auch dieses Jahr wieder der europäische Kongress der Hämatologen im Hybridformat. Mit spannenden Vorträgen und Workshops, u.a. zu den optimalen Therapiestrategien bei der CLL.
Programm und weitere Informationen
- The Surveillance, Epidemiology, and End Results (SEER) Program of the National Cancer Institute. Cancer Stat Facts: Leukemia-Chronic Lymphocytic Leukemia (CLL). Online unter: https://seer.cancer.gov/statfacts/html/clyl.html (letzter Zugriff: Mai 2023).
- Barf T et al. Acalabrutinib (ACP-196): A Covalent Bruton Tyrosine Kinase Inhibitor with a Differentiated Selectivity and In Vivo Potency Profile. J Pharmacol Exp Ther 2017;363:240-52.
- Wendtner CM et al. Onkopedia-Leitlinie Chronische Lymphatische Leukämie (CLL). Stand: Januar 2023. Online unter: https://www.onkopedia.com/de/onkopedia/guidelines/chronische-lymphatische-leukaemie-cll/@@guideline/html/index.html (letzter Zugriff: Mai 2023).
- Hilal T et al. Adverse Events in Clinical Trials of Ibrutinib and Acalabrutinib for B-Cell Lymphoproliferative Disorders: A Systematic Review and Network Meta-Analysis. ASH 2020, Abstract 1317.
- Byrd JC, Hillmen P, Ghia P, et al. Acalabrutinib versus ibrutinib in previously treated chronic lymphocytic leukemia: results of the first randomized phase III trial. J Clin Oncol. 2021;39(31):3441–3452.
- Hiller E. „Entwicklung weniger toxischer BTK-Inhibitoren ist begrüßenswert“. Kommentar zu Y. Byrd JC, Hillmen P, Ghia P, et al. Acalabrutinib versus ibrutinib in previously treated chronic lymphocytic leukemia: results of the first randomized phase III trial. J Clin Oncol. 2021;39(31):3441–3452. InFo Hämatologie + Onkologie 2022;25(12):32.
- Kuss B, Nagarajan C, Hsieh WS, Cheah CY. Practical management of chronic lymphocytic leukemia with acalabrutinib. Leuk Lymphoma. 2022 Dec;63(12):2785-2794. doi: 10.1080/10428194.2022.2098289. Epub 2022 Jul 19. PMID: 35852229.
- ClinicalTrials.gov Identifier: NCT02950051
- CLL: Neue Zweifach- und Dreifachkombinationen machen das Rennen. Interview mit Prof. Dr. Clemens Wendtner (München) im Rahmen des EHA 2022. Online unter: https://www.krebsgesellschaft.de/onko-internetportal/kongresse/eha-icml/zweifach-und-dreifachkombinationen-bei-cll-eha-2022.html (letzter Zugriff: Mai 2023).
Abkürzungen:
BCL = B-Cell lymphoma
BTK = Bruton-Tyrosinkinase
BTKi = Bruton-Tyrosinkinase-Inhibitor
CLL = Chronische lymphatische Leukämie
EHA = European Hematology Association (bzw. deren Jahreskongress)
 Abbildung 1: Erstlinientherapie der CLL. Adaptiert nach: Onkopedia-Leitlinie CLL. Stand: Januar 2023, letzter Zugriff: Mai 2023.3
Abbildung 1: Erstlinientherapie der CLL. Adaptiert nach: Onkopedia-Leitlinie CLL. Stand: Januar 2023, letzter Zugriff: Mai 2023.3
 Abbildung 2: Therapie der CLL bei Rezidiv und Refraktärität. Adaptiert nach: Onkopedia-Leitlinie CLL. Stand: Januar 2023, letzter Zugriff: Mai 2023.3
Abbildung 2: Therapie der CLL bei Rezidiv und Refraktärität. Adaptiert nach: Onkopedia-Leitlinie CLL. Stand: Januar 2023, letzter Zugriff: Mai 2023.3
