Partikeltherapie als hochpräzise Technologie im Kampf gegen Krebs
Können Kohlenstoffionen den Kampf gegen Krebs revolutionieren? Ein Experte für Kernphysik erläutert die Partikeltherapie genauer.
Partikeltherapie: Hohe Ladungen und extreme Präzision zur Bekämpfung von strahlungsresistenten Tumoren
Übersetzt aus dem Französischen
Es gibt drei Hauptarten der Krebsbehandlung, die einzeln oder in Kombination erfolgen können: chirurgische Eingriffe, Chemotherapie und Strahlentherapie. Letztere besteht in der Anwendung ionisierender Strahlung (hauptsächlich Röntgen- oder Elektronenstrahlen, mitunter aber auch innere radioaktive Quellen) bei der lokalen oder lokal-regionalen Behandlung von Krebstumoren. Dabei soll die vorgeschriebene Dosis auf den Tumorbereich gerichtet werden, während das umliegende gesunde Gewebe so weit wie möglich geschont wird.
Trotz großer Fortschritte bei der Strahlenqualität und -formung können jedoch bestimmte Tumorarten, die als "strahlenresistent" gelten (ca. 2% der Fälle), nicht mit konventioneller Strahlentherapie behandelt werden.
Tumore mit Protonen und Kohlenstoffionen bestrahlen
Es gibt eine alternative und zunehmend vielversprechende Behandlungsmethode für diese Art von strahlenresistenten Tumoren. Bei der Partikeltherapie, auch Hadronentherapie genannt, werden Tumore nicht mit Röntgenstrahlen (Photonen) bestrahlt, sondern mit geladenen Teilchen wie Protonen oder sogar Kohlenstoffionen. Der große Unterschied zwischen Photonen und diesen geladenen Atomkernen ist die Art und Weise, wie diese beiden Partikelarten ihre Energie im Körper des Patienten abgeben.
Obwohl die Protonentherapie recht bekannt ist (es gibt etwa 100 Behandlungszentren weltweit, darunter drei in Frankreich), handelt es sich bei der Kohlenstofftherapie noch um eine relativ unbekannte Technologie. In der Theorie umfasst der Begriff "Partikeltherapie" diese beiden Techniken. In der Praxis bezieht er sich eher auf die letztere.
Kohlenstofftherapie: beispiellose Präzision
Während Röntgenstrahlen auf ihrem Weg vom Eintritt bis zum Austritt aus dem Körper des Patienten Energie abgeben, dringen geladene Teilchen (Protonen oder Kohlenstoff-Ionen) nur bis zu einer bestimmten Tiefe ein und dann nicht weiter. Die Eindringtiefe variiert je nach der Energie des Strahls und der Beschaffenheit des Stoffs, den er durchdringt.
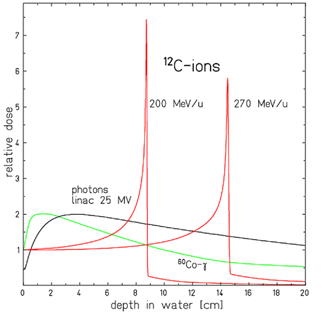
Vergleich der unterschiedlichen Profile der Dosisabgabe für zwei Kohlenstoff-Ionenstrahlen mit unterschiedlicher Energie (in rot) und zwei Röntgenstrahlen (in grün und schwarz). D. Schardt et al., Reviews of Modern Physics, 82 (2010), 383
Außerdem verläuft die Energieabgabe von Röntgenstrahlen mit zunehmender Tiefe entlang eines leicht abnehmenden Profils (ein einzelner Strahl gibt also in der Nähe der Oberfläche mehr Energie ab als im Tumor in der Tiefe). Im Gegensatz dazu geben geladene Teilchen auf ihrem Weg nur sehr wenig Energie ab.
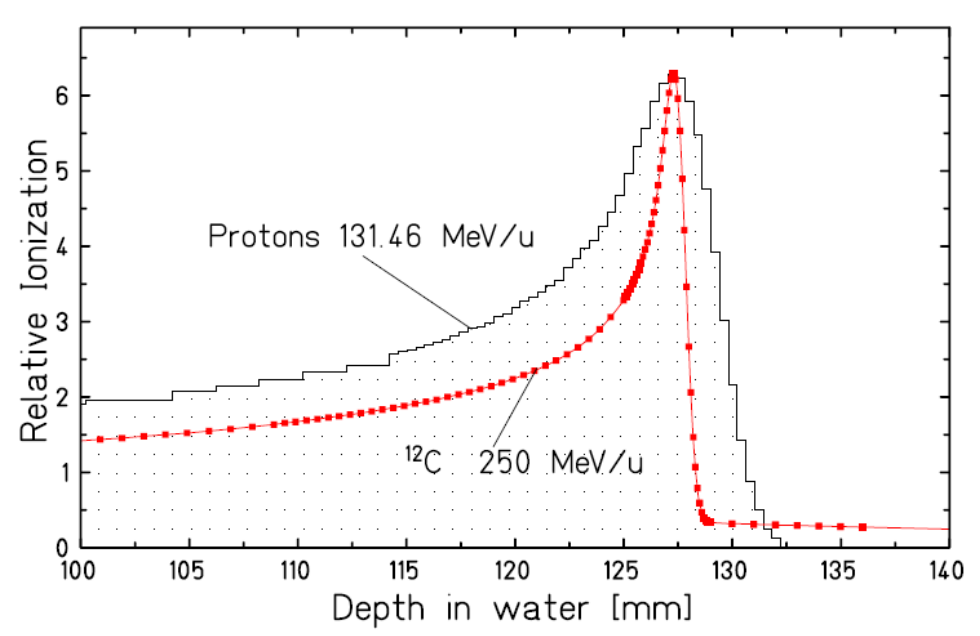
Ihre Wechselwirkung mit dem Gewebe, das sie durchqueren, zeichnet sich jedoch durch eine Spitze der Energieabgabe (den sogenannten "Bragg-Peak") in der Nähe der Stelle aus, an der sie anhalten. Da die räumliche und energetische Streuung von Kohlenstoff-Ionen geringer ist als die von Protonen, ist der mit der Kohlenstoff-Therapie erzielte Bragg-Peak bei gleicher Tiefe sogar noch präziser als bei der Protonentherapie.
Vergleich des Bragg-Peaks eines Kohlenstoff-Ionenstrahls und eines Protonenstrahls auf gleicher Bahn. Der Bragg-Peak des Protonenstrahls ist etwa dreimal so breit.
Es ist wenig verwunderlich, dass das Interesse an dieser Art der Bestrahlung rasch zunimmt. Immerhin kann sie die Energieabgabe im Gewebe vor dem Tumor erheblich reduzieren, im Gewebe nach dem Tumor praktisch aufheben und die Dosis genau in der Tiefe, in der sich der Tumor befindet, maximieren.
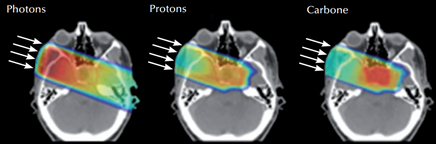
©GCS ETOILE - Wirkung eines einzelnen Strahls bei der Röntgenbestrahlung (links), der Protonentherapie (Mitte) und der Kohlenstoffpartikeltherapie (rechts). Der Tumor liegt in der Mitte des Schädels.
Die Vorteile der Partikeltherapie
Hohe Effektivität bei strahlenresistenten Tumoren
Die Partikeltherapie eignet sich besonders für strahlenresistente Tumore wie Gallengangskarzinome oder Bauchspeicheldrüsenkrebs. Erstaunlicherweise reagieren diese Tumore mitunter sehr empfindlich auf diese neue Art von Strahlung, die dann zusätzlich zur konventionellen Strahlentherapie eingesetzt wird.
Eine Therapie mit hoher Treffgenauigkeit
Einer der weiteren Vorteile ist die hohe Treffgenauigkeit. Der Partikelstrahl endet nicht nur im Tumor und lässt das dahinter liegende Gewebe vollständig unberührt, er ist auch viel dünner als ein Röntgenstrahl. Daher muss der Strahl während der Behandlung bewegt werden, um den Tumor Punkt für Punkt in seiner gesamten Größe zu bestrahlen. Diese hohe Präzision ist von unschätzbarem Wert bei der Behandlung von Tumoren, die sehr nahe an strahlenempfindlichem gesundem Gewebe liegen, wie z. B. Rückenmarks- und paraspinale Tumore: Sarkome und inoperable oder unvollständig herausgeschnittene Chordome.
Die Wirksamkeit der Partikeltherapie übertrifft andere Behandlungen
Darüber hinaus zeigen die für die Kohlenstoff-Ionen-Bestrahlung veröffentlichten Ergebnisse eine Wirksamkeit weit über den Werten von Behandlungen ohne Kohlenstoff. Diese Ergebnisse betreffen Adenokarzinome im Kopf- und Halsbereich, Schleimhautmelanome, Chordome, Sarkome, Leberkarzinome und rezidivierende Rektaladenokarzinome im Beckenbereich.
Eine kürzere Therapie
Nicht zuletzt wird durch den Einsatz der Kohlenstofftherapie auch die Anzahl der erforderlichen Sitzungen verringert. Daten aus Italien zeigen, dass für die Behandlung mit Protonen durchschnittlich 35 Sitzungen erforderlich sind, während es bei der Behandlung mit Kohlenstoff-Ionen nur 16 sind.
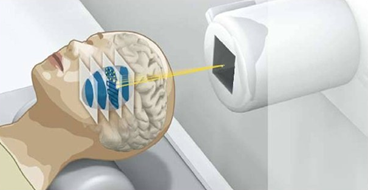
©GSI - Abbildung der "Rasterscan"-Methode, die eine Behandlung des gesamten Tumors durch Variieren der x-, y- und z-Position des Bragg-Peaks ermöglicht.
Welche Einschränkungen hat die Partikeltherapie?
Schwierigkeiten bei bewegendem Tumor
Eine Einschränkung der Partikeltherapie besteht darin, dass ein sich bewegender Tumor nicht in Echtzeit verfolgt werden kann, wenn sich seine Position mit der Atmung des Patienten ändert (Lunge, Leber, Bauchspeicheldrüse usw.). Ein Lösungsansatz für dieses Problem besteht darin, den Patienten einem 4D-Scan zu unterziehen, wobei die vierte Dimension die Atemzeiten sind. Dadurch sollen die Bewegungen des Tumors beim Ein- und Ausatmen "fotografiert" werden. Während der Behandlung verfolgen Infrarotkameras den Tumor mit Sensoren, die am Patienten angebracht sind, und der Strahl wird nur dann aktiviert, wenn sich der Tumor in einer Position befindet, in der der Strahl ihn erreichen kann.
Logistik: die größte Einschränkung der Partikeltherapie
Die größte Einschränkung ist jedoch natürlich logistischer Natur. Die Partikeltherapie mit Kohlenstoff-Ionen erfordert einen Teilchenbeschleuniger in unmittelbarer Nähe des Behandlungsraums. Eine weitere Voraussetzung ist ein bewegliches Element, das sich um den Patienten drehen kann, ohne die millimetergenaue Präzision zu beeinträchtigen. Eine Anlage dieser Größe ist angesichts der Dimensionen, der technischen Schwierigkeiten und der erforderlichen Investitionen sicherlich eine Herausforderung.
Einer der Gründe für die geringe Anzahl von Standorten für die Kohlenstoff-Ionentherapie sind die Kosten. Derzeit gibt es in Europa nur vier Standorte für die Kohlenstoffpartikeltherapie: zwei in Deutschland (das Heidelberger Ionenstrahl-Therapiezentrum, HIT, und das Marburger Ionenstrahl-Therapiezentrum, MIT), einen in Österreich (MedAustron in der Wiener Neustadt) und einen in Italien (Centro Nazionale di Adroterapia Oncologica, CNAO).

©CNAO - Das CNAO-Synchrotron befindet sich in einem 1.600 m² großen Bunker und ist durch einen zwei bis sechs Meter dicken Strahlungsschild aus Stahlbeton vom Rest des Gebäudes abgeschirmt. Protonen und Kohlenstoff-Ionen werden durch Magnetfelder isoliert, bevor sie im linearen Teil (6 Meter lang, in rosa) eine erste Beschleunigung erfahren.

©GSI - Die rotierende "Gantry" (blau) in Heidelberg ist ebenso beeindruckend. Sie trägt einen Teil des Kohlenstoff-Ionen-Beschleunigers (orange), sodass sich der Strahl um den Patienten im Behandlungsraum drehen kann (hier nicht sichtbar).
Die Kohlenstoff-Ionen-Partikeltherapie zusammengefasst
Die Kohlenstoff-Ionen-Partikeltherapie ist eine innovative und hochwirksame Technologie zur Behandlung von strahlenresistenten Tumoren, die eine komplexe Struktur aufweisen oder ungünstig im Körper des Patienten liegen. Allerdings ist das Verfahren extrem komplex, und das behindert seine Entwicklung erheblich. Während Japan mit sieben Behandlungszentren für die Kohlenstofftherapie ein Pionier auf diesem Gebiet ist, mangelt es in Frankreich noch an entsprechenden Einrichtungen.