a Olumiant® (Baricitinib) wird angewendet zur Behandlung von mittelschwerer bis schwerer aktiver rheumatoider Arthritis bei erwachsenen Patienten, die auf eine vorangegangene Behandlung mit einem oder mehreren krankheitsmodifizierenden Antirheumatika (DMARD) unzureichend angesprochen oder diese nicht vertragen haben. Baricitinib kann als Monotherapie oder in Kombination mit Methotrexat angewendet werden.2
b Hierbei handelt es sich um Daten aus der Behandlungsrealität, die nicht in randomisierten, kontrollierten und konfirmatorischen Studien, sondern ergänzend zu diesen Daten erhoben wurden.
c Die Studie beinhaltet eine Analyse von RWD von Personen mit aktiver RA unter Baricitinib (932 in Monotherapie, 850 in Kombination mit csDMARD) aus den Patientengruppen der RA-BE-REAL-Studie, der Erlangen-Baricitinib-Kohorte, der Studie SUSTAIN, dem BSRBR-RA-Register, dem Schweizer Register SCQM und der Studie ORBIT-RA. Es wurde keine statistische Modellierung angewendet und alle Analysen waren deskriptiv. Limitationen: unterschiedliches Design der einzelnen Register und Studien sowie in Bezug auf die Fortführung/ Absetzung von Medikamenten, kleine Kohorte sowie z. T. fehlende/ unterschiedliche Daten zu den Patienten.
d Die Studie RA-BE-REAL ist eine auf 3 Jahre ausgelegte prospektive Beobachtungsstudie, welche die Wirksamkeit und Zeit bis zum Abbruch der ersten RA-Behandlung untersucht: Patienten innerhalb Europas (EU-Kohorte: Deutschland, Frankreich, Großbritannien, Spanien und Italien) wurden über 3 Jahre und Patienten außerhalb Europas (Nicht-EU-Kohorte: Australien, Kanada und Saudi-Arabien) über 2 Jahre beobachtet; n=1.322, Gruppe A wurde mit Baricitinib 2 oder 4 mg behandelt, Gruppe B wurde mit einem ts/bDMARD behandelt.
e In der LTE-Studie waren 996 Patienten aus vorangegangenen Phase-III-Studien eingeschlossen, die 15 Monate oder länger mit Baricitinib 4 mg behandelt wurden und eine LDA oder eine Remission nach dem CDAI aufrechterhielten. Sie wurden blind randomisiert und erhielten entweder weiter die 4 mg Dosierung Baricitinib oder wurden auf 2 mg reduziert. Setzte unter Dosisreduktion die Krankheitsaktivität wieder ein, konnte die Dosis erneut auf 4 mg gesteigert werden (Rescue Therapie).
f Dosis anpassbar entsprechend der Krankheitsaktivität. Empfohlene Dosis 4 mg; 2 mg sind für bestimmte Patientenpopulationen angebracht, siehe Fachinformation.2
g Die Ergebnisse sind statistisch signifikant, wenn 1 nicht durch das 95 %-Konfidenzintervall für die rHR abgedeckt ist. Aufgrund des geringen Stichprobenumfangs wurden Patienten, die nicht ein TNFi oder ein tsDMARD erhielten, als OMA gepoolt. OMA=anderer Wirkmechanismus (Other Mechanism of Action); rHR=eingeschränkte Hazard Ratio (restricted Hazard Ratio).
h BARE-BONE war eine prospektive, einarmige, interventionelle, offene, monozentrische Phase-IV-Studie, welche die Wirksamkeit von Olumiant® (4 mg) auf die Beschaffenheit der Knochen bei 27 Patienten mit mittelschwerer bis schwerer aktiver RA während 52 Wochen untersuchte (Effekte über 52 Wochen hinaus noch nicht untersucht).
i Zweiseitige p-Werte von weniger als 0,05 oder zweiseitige 95%-Konfidenzintervalle von Regressionskoeffizienten, die 0 ausschließen, wurden als signifikant angesehen.
j Kleine Teilnehmerzahl japanischer Patienten (n=122), Ergebnisse daher evtl. nicht auf RA-Patienten anderer Ethnizitäten anwendbar.
JAK-Inhibition: RA-Therapie im Realitätscheck – ein Update zum RhK 2025
Neueste Erkenntnisse aus dem klinischen Alltag zu JAK-Inhibitoren und deren Wirksamkeit waren Themen im Lilly-Symposium auf dem diesjährigen Deutschen Rheumatologie Kongress. Renommierte Expert:innen stellten die Therapieoption bei rheumatoider Arthritis<sup>a</sup> ins Licht aktueller Real-World-Daten (RWD)<sup>b</sup>.

Dr. Christina Gebhardt (München), Dr. Silke Zinke (Berlin) und Prof. Dr. Dr. Axel Hueber (Nürnberg) präsentierten unter dem Vorsitz von Prof. Dr. Torsten Witte (Hannover) neueste RWD und diskutierten aktuelle Erkenntnisse aus dem Versorgungsalltag im Hinblick auf eine langfristig wirksame RA-Therapie.
Lift-off: Monotherapie startet durch
Die Anwendung von Januskinase(JAK)-Inhibitoren sowie Interleukin(IL)-6-Inhibitoren ist gemäß aktueller Leitlinien in Monotherapie oder in Kombination mit Methotrexat (MTX) für die Behandlung der rheumatoiden Arthritis (RA) empfohlen.1 Für den Praxisalltag diskutierte Frau Dr. Gebhardt die Frage „Sind die Wirkstoffe gleich effektiv in Mono- wie auch in Kombinationstherapie?“ Zum Januskinase-(JAK)-Inhibitor Baricitinib (Olumiant®)2 in Monotherapie klärte die Expertin auf und präsentierte eine Analysec 6 internationaler Studien aus RWD. Dabei war die Wirksamkeit von Baricitinib in Monotherapie mit der in Kombinationstherapie vergleichbar.3 So zeigte sich in der SUSTAIN-Studie und der spanischen Studie ORBIT-RA nach einem Jahr, dass ein vergleichbarer Anteil an Patient:innen eine Remission oder niedrige Krankheitsaktivität (Low Disease Activity; LDA) nach CDAI-Kriterien (Clinicial Disease Activity Index) erreichen konnte.3 „Im Schweizer Register SCQM-RA konnte sogar ein deutlich höherer Anteil an Patient:innen in Remission oder LDA unter Monotherapie verglichen mit der Kombinationstherapie festgestellt werden.“3 Überdies geht aus der in die Analyse eingeschlossene RA-BE-REALd-Studie im Real-World-Setting hervor, dass die Anwendung einer Monotherapie im Alltag angekommen ist: In allen Untergruppen erhielten mehr Baricitinib-Patient:innen den Wirkstoff in Monotherapie als Patient:innen, die mit Tumornekrosefaktor-Inhibitor(TNFi)- und Nicht-TNFi-haltigen Wirkstoffen behandelt wurden.4
„Wir können mit Baricitinib auch in der Monotherapie Therapieziele wie eine Remission oder LDA, die wir uns im Behandlungsalltag stecken, erreichen“, statuierte Dr. Gebhardt.
Mission in die Remission – bei optimaler Dosierung
Der Frage, wie in der Praxis hinsichtlich einer Dosisreduktion gehandelt wird, begegnete Dr. Gebhardt offen: „Wenn eine anhaltende Remission mit Baricitinib erreicht wurde, dürfen wir uns trauen, die Dosis zu reduzieren – immer mit Blick auf die Zulassung“, so die Referentin. Denn aktuelle Ergebnisse der RA-BEYONDe-Studie zeigen, dass 60 % der Patient:innen eine Remission oder LDA auch unter reduzierter Dosis von 2 mgf nach 96 Wochen aufrechterhalten konnten (versus 70 % mit 4 mg Baricitinib kontinuierlich).5
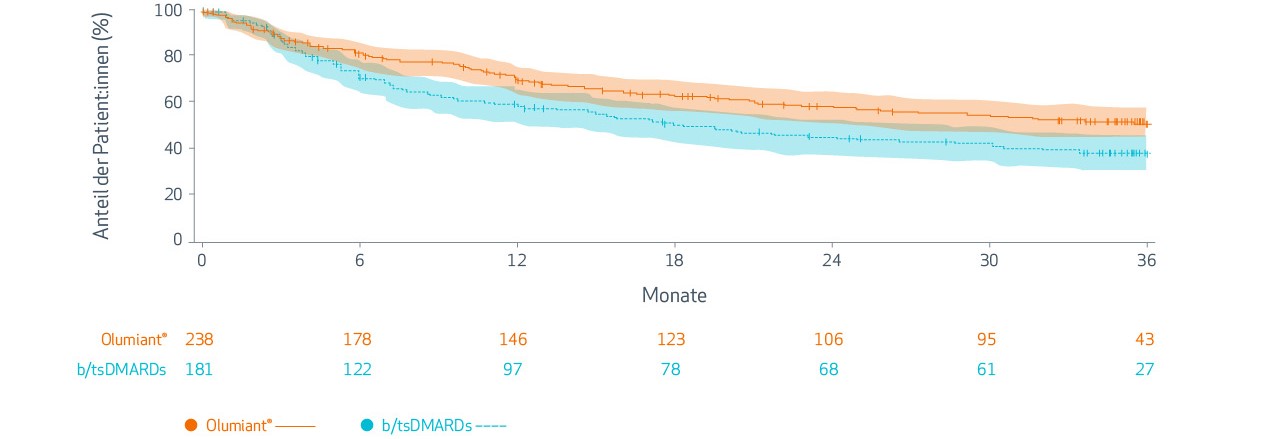
Die Erfolge einer Langzeittherapie in reduzierter Dosierung verdeutlichte Dr. Silke Zinke an einem realen Patientenfall. Nach knapp 7 Jahren Krankheitsdauer, unzureichend wirksamer Therapieansätze und einer Unverträglichkeit gegenüber MTX stellte Dr. Zinke ihre Patientin auf Baricitinib in Monotherapie ein. „Meine Patientin befindet sich seit nun 6 Jahren unverändert in Remission, auch nach einer Dosisreduktion von 4 auf 2 mg.“ Und führte aus: „Der Patientenfall zeigt genau das, was wir in der Realität sehen wollen, und zwar, dass die Patient:innen lange keine Krankheitsaktivität haben. Zudem wird auch die hohe Therapietreue unter Baricitinib deutlich.“ Zur Therapieadhärenz liefert auch die RA-BE-REAL-Studie überzeugende Ergebnisse: Nach zwei Jahren konnte unter Baricitinib eine um 50 % höhere Therapiepersistenz im Vergleich zu TNFi festgestellt werden.g,4 Neueste auf dem RhK präsentierte Auswertungen der Deutschen Kohorte bekräftigen dies: Über den Beobachtungszeitraum von 3 Jahren verblieben unter Baricitinib mehr Patient:innen auf Therapie im Vergleich zu anderen b/tsDMARDs (56,4 % vs. 43,3 %) (Abb.1).6
In andere Sphären: Knochengesundheit
Raus aus dem Makrokosmos mit Kurs auf die kleineren Strukturen ging es abschließend auf die Reise zur Knochengesundheit. Welche Schäden eine RA am Knochen verursachen kann, wurde durch hochauflösende periphere quantitative CT-Aufnahmen der Knochen von Patient:innen mit aktiver RA (n=27) der BARE-BONEh-Studie deutlich.7 Anhand von Scans der Speiche zu Studienbeginn, in Woche 24 und 52 wurde in der Studie die Veränderung der Knochenfestigkeit bewertet: Unter Baricitinib verbesserte sich die geschätzte Bruchlast und Steifigkeit des Knochens im Vergleich zu Baseline signifikanti (Abb. 2). Dies ging mit einer Abnahme der kortikalen Porosität einher und deutet auf eine verbesserte Festigkeit und Elastizität der Knochen hin. Die BARE-BONE-Studie stellt so heraus, dass Baricitinib zur konsistenten Verbesserung von Knocheneigenschaften beitragen kann.
Zirkadianer Rhythmus – Baricitinib zur optimalen Zeit
Abschließend erweiterte die Frage „Wann ist der optimale Zeitpunkt, Baricitinib einzunehmen?“ den Horizont. Hierzu liegen aktuelle Ergebnisse einer japanischen Studiej vor, die unterstreichen, dass eine abendliche Einnahme von Baricitinib die Wirkung positiv beeinflussen kann.8 In der nicht-randomisierten und kontrollierten Studie mit 122 Patient:innen über 52 Wochen wurde festgestellt: Patient:innen, die Baricitinib (4 mg) am Abend (BAR4EVE) erhielten, zeigten ein schnelleres Ansprechen auf den Wirkstoff als diejenigen, die Baricitinib (4 mg) morgens (BAR4MORN) einnahmen – mit den größten Unterschieden zwischen Woche 4 und Woche 12.8 Zudem zeigte sich ein signifikant besseres ACR20-Ansprechen in der BAR4EVE-Gruppe in Woche 12 im Vergleich zur BAR4MORN-Gruppe (78,2 % vs. 43,3 %; p < 0,001).8 „Ich konnte an Fällen in meiner Praxis bereits beobachten, dass eine Umstellung zur abendlichen Einnahme Symptome wie die Morgensteifigkeit nochmal besser reduzieren konnte“, berichtete Dr. Zinke.
Fazit
Die aktuellen Erkenntnisse der RA-BE-REAL-Studie verdeutlichen den langfristigen Erfolg einer JAK-Inhibition mit Baricitinib: RA-Patient:innen konnten von einer über Jahre anhaltenden Remission profitieren, die sich in einer hohen Therapietreue widerspiegelte.4,6 Überdies weisen neueste klinische Daten darauf hin, dass die abendliche Einnahme von Baricitinib die Wirksamkeit positiv beeinflussen kann. Zusammen mit den Hinweisen auf einen positiven Effekt der abendlichen Einnahme wurde deutlich: Baricitinib hat sich als bewährte Therapieoption positioniert – auch in Monotherapie.3,8
Abb. 1: RA-BE-REAL: Höhere Therapieadhärenz bei Patient:innen unter Baricitinib verglichen mit b/tsDMARDs der deutschen Kohorte nach 3 Jahren. Mod. nach 6.
Abb. 2: BARE-BONE: Verbesserung der Knochenfestigkeit in Woche 52 im Vergleich zum Ausgangswert. Mod. nach 7.
© Lilly Deutschland in Kooperation mit dem Universitätsklinikum Erlangen. ** veranschaulicht durch strukturelle Veränderungen in den MCP-Gelenken und der Speiche sowie Veränderungen der biomechanischen Eigenschaften bei zwei Patient:innen.
Fußnoten
Quellen
- Smolen J, et al. Ann Rheum Dis 2023: 82:3-18
- Fachinformation Olumiant®; aktueller Stand. Im Internet: https://www.fachinfo.de/fi/pdf/021493; 19.09.2025
- Edwards CJ, et al. CMRO 2024; 40(11): 1993-2002
- Alten R, et al. Rheumatol Ther 2023; 10: 1575-95
- Edwards CJ, et al. The Journal of Rheumatology 2025;52:316-22
- Alten R et al. presented at RhK 2025; Poster RA.21.
- Simon D et al. Arthritis Rheumatol 2023; DOI: 10.1002/art.42617.
- Hashimoto T et al., Arthritis Res Ther 2025; 27:91.
PP-BA-DE-4945