* ATTR-ACT war eine multizentrische, internationale, placebokontrollierte, doppelblinde, randomisierte Phase-III-Parallelgruppen-Studie an 441 Patient:innen mit Wildtyp- oder hereditärer ATTR-CM. In ATTR-ACT wurden Patient:innen mit ATTR-CM per Randomisierung (2:1:2) einer Behandlung mit Vyndaqel® 80 mg, Vyndaqel® 20 mg oder Placebo einmal täglich über 30 Monate zugewiesen. Die Behandlung mit Vyndaqel® war mit einer relativen Risikoreduktion der Gesamtmortalität um 30 % nach 30 Monaten gegenüber Placebo assoziiert. In der Langzeiterweiterungsstudie war die kontinuierliche Behandlung mit Vyndaqel® mit einer relativen Risikoreduktion der Gesamtmortalität um 41 % nach 5 Jahren gegenüber Patient:innen verbunden, die in den ersten 30 Monaten Placebo erhielten.2,4,13
** Vyndaqel® (Tafamidis) 61 mg und Vyndaqel® (Tafamidis-Meglumin) 80 mg sind indiziert zur Behandlung der Wildtyp-oder hereditären Transthyretin-Amyloidose bei erwachsenen Patient:innen mit Kardiomyopathie.13 Eine einzelne Kapsel Vyndaqel® 61 mg ist bioäquivalent zu Vyndaqel® 80 mg (vier Kapseln zu 20 mg). Diese sind auf Basis der mg-Angabe nicht gegeneinander austauschbar.13,14
*** Es gibt gegenwärtig keine wissenschaftliche Evidenz dafür, dass ein Wechsel oder eine Kombination von ATTR-CM-Therapien zu einer Verbesserung der klinischen Ergebnisse führt.1
¥ Post-hoc-Analyse der ATTR-ACT-Studie und LTE nach NAC Stadium mit bis zu 90 Monaten Follow-up. Weder ATTR-ACT noch die LTE-Studie waren statistisch darauf ausgelegt, die Wirkung von Tafamidis 80 mg/61mg* nach NAC Stadium zu untersuchen; daher sind die Ergebnisse explorativ. In der Post-hoc Analyse zeigten sich statistisch signifikante Effekte für Mortalität und kardiovaskuläre Hospitalisierungen in den NAC Stadien I und II, während für NAC Stadium III lediglich numerisch günstige, jedoch nicht statistisch signifikante Trends beobachtet wurden.
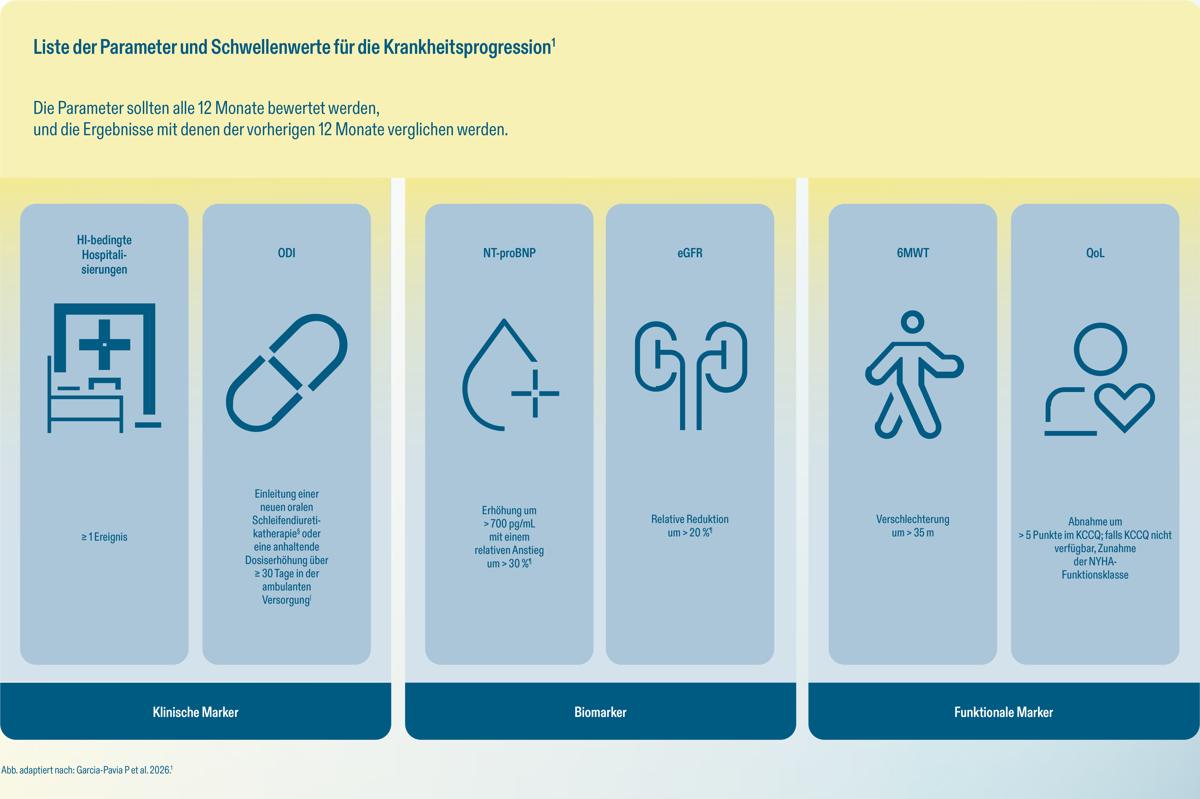
‡ Die Krankheit galt als stabil, wenn die Kriterien für eine Progression nicht erfüllt wurden (Verschlechterung sowohl von NT proBNP als auch ODI).5
† Bei Interpretation und Anwendung der Kriterien in der Praxis werden klinisches Urteilsvermögen sowie die Berücksichtigung patientenspezifischer Faktoren empfohlen.
§ Bei Patient:innen, die keine Schleifendiuretika einnehmen.1
I Bei Patient:innen, die Diuretika einnehmen.1
¶ Die Messung sollte in einer Phase klinischer Stabilität erfolgen. Alternativ können zwei Messungen im Abstand von etwa 4 Wochen dazu beitragen sicherzustellen, dass vorübergehende Veränderungen nicht fälschlicherweise als Progression gewertet werden.1
# Behandelte Patient:innen hatten eine weniger schwere Erkrankung als unbehandelte Patient:innen, was durch einen niedrigeren medianen NT proBNP Wert angezeigt wurde, und wurden häufiger ab 2019 in THAOS eingeschlossen.10
- Garcia Pavia P et al. JACC Heart Fail.2026;14(1):102766.
- Maurer MS et al. N Engl J Med. 2018;379(11):1007–1016.
- Maurer MS et al. JACC Basic Transl Sci. 2018;3(6):871–873.
- Elliott P et al. Circ Heart Fail. 2022;15(1):e008193.
- Garcia-Pavia P et al. Disease stabilization in patients with ATTR-CM during the first year of tafamidis treatment. Poster präsentiert auf: American College of Cardiology Annual Scientific Session & Expo (ACC 2025); 29.–31. März 2025; Chicago, IL.
- Ioannou A et al. J Am Coll Cardiol. 2024;83(14):1276–1291.
- Garcia-Pavia P et al. Eur Heart J. Online publiziert: 7. Oktober 2025.
- Rettl R et al. Eur Heart J Cardiovasc Imaging. 2022;23(6):767–780.
- Damy T et al. Eur J Heart Fail. Online publiziert: 9. Juni 2025.
- Garcia-Pavia P et al. J Card Fail. 2025;31(3):525–533.
- Grogan M et al. Eur J Heart Fail. 2024;26(3):612–615.
- Garcia-Pavia P et al. JACC Heart Fail. 2024;12(1):150–160.
- Fachinformation Vyndaqel® 61 mg, aktueller Stand.
- Lockwood PA et al. Clin Pharmacol Drug Dev. 2020;9(7):849–854.
- Garcia-Pavia P et al. Disease stabilization in patients with Transthyretin amyloid cardiomyopathy during the first year of tafamidis treatment. (Abstract) JACC. 2025, 85 (12_Supplement) 1338.