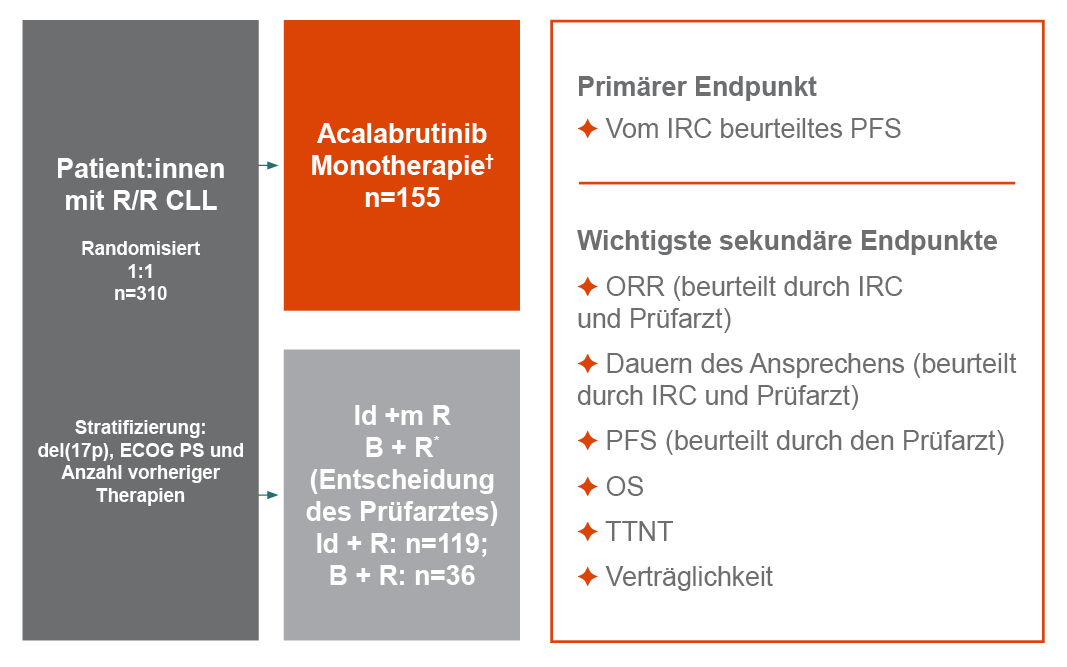
B + R = Bendamustin + Rituximab; del(17p) = 17p-Deletion; ECOG PS = Eastern Cooperative Oncology Group Performance Status; Id + R = Idelalisib + Rituximab; IRC = unabhängiger Untersuchungsausschuss; ORR = Gesamtansprechrate; OS = Gesamtüberleben; PFS = progressionsfreies Überleben; R/R CLL = rezidivierte/refraktäre CLL; TTNT = Zeit bis zur nächsten Behandlung† Acalabrutinib100 mg zweimal täglich bis zur Krankheitsprogression oder nicht akzeptablen Toxizität.
Update der ASCEND-Studie: Acalabrutinib auch nach 3 Jahren wirksam
Acalabrutinib hat sich bereits im ersten Jahr nach seinem Launch als wichtige Option in der CLL-Therapie etabliert. Das Langzeit-Follow-up der ASCEND-Studie ergänzt und bestätigt die solide Evidenzbasis für den Einsatz des BTKi der 2. Generation
Acalabrutinib hat sich bereits im ersten Jahr nach seinem Launch als wichtige Option in der CLL-Therapie etabliert. Das Langzeit-Follow-up der ASCEND-Studie ergänzt und bestätigt die solide Evidenzbasis für den Einsatz des BTKi der 2. Generation.
Bei der leitliniengerechten Therapie der chronischen lymphatischen Leukämie (CLL) hat sich in den vergangenen Jahren ein Paradigmenwechsel zugunsten zielgerichteter Optionen vollzogen. Bruton-Tyrosinkinase-Inhibitoren (BTKi) gehören neben BCL2-Inhibitoren in allen Indikationssegmenten, unabhängig vom Vorliegen genetischer Hochrisikomerkmale, zur empfohlenen Standardtherapie.1
Im Unterschied zu BCL2-Inhibitoren wie Venetoclax, dessen Einsatz immer in Kombination mit einem Anti-CD20-Antikörper erfolgt, werden die BTKi in der Erstlinie optional mit Anti-CD20-AK und ansonsten als Monotherapie angewendet, was insbesondere in Zeiten der COVID-19-Pandemie als vorteilhaft erscheint.1 Bei rezidivierter oder refraktärer CLL (R/R CLL) zeigen BTK-Hemmer auch nach einer Vortherapie mit Venetoclax eine sehr gute Wirksamkeit.1
Zweiter BTK-Inhibitor mit höherer Selektivität
Seit November 2020 steht mit Acalabrutinib (Calquence®) ein weiterer BTKi zur Verfügung.2 Seine Entwicklung erfolgte angesichts des einsatzlimitierenden Toxizitätsprofils von Ibrutinib mit dem Fokus auf einer höheren Selektivität. Schon vor seiner EMA-Zulassung wurde der potente BTKi der 2. Generation im September 2020 in die aktuelle Version der Onkopedia-Leitlinie1 aufgenommen (Kurzvideo: Praxisupdate Onkopedia Leitlinie CLL). Die Grundlage für Zulassung und Leitlinienempfehlung bilden die Phase-III-Studien ELEVATE TN3 (Erstlinientherapie) und ASCEND4 (Rezidivtherapie).
Die ASCEND-Studie diente zur Untersuchung der Wirksamkeit und Verträglichkeit einer Monotherapie mit Acalabrutinib im Vergleich mit der Kombination aus dem PI3K-Inhibitor Idelalisib plus Rituximab (IdR) bzw. der Chemoimmuntherapie mit Bendamustin plus Rituximab (BR) bei Patienten mit R/R CLL (s. Abb. 1).4 Dabei handelt es sich um die erste randomisierte Studie mit CLL-Patienten, in der – neben dem Vergleich mit einer Standard-Chemoimmuntherapie – zwei zielgerichtete Behandlungsoptionen miteinander verglichen wurden. Die Therapiewahl zwischen IdR und BR erfolgte nach Prüfarztentscheidung und fiel bei über drei Viertel der Patient:innen im Vergleichsarm zugunsten von IdR aus.4
ASCEND: Studiendesign und Endpunkte
Die Primäranalyse der ASCEND-Studie erfolgte nach einer medianen Nachbeobachtungszeit von rund 16 Monaten. Die Monotherapie mit Acalabrutinib führte bei Patient:innen mit R/R-CLL in allen Subgruppen – auch bei Vorliegen genetischer Risikofaktoren – zu einem PFS-Vorteil im Vergleich mit den beiden Kombinationstherapien (IdR bzw. BR). Unter Acalabrutinib waren nach einem Jahr noch 88 % der Patient:innen progressionsfrei gegenüber 68 % in der Vergleichsgruppe. Das mediane PFS – der primäre Studienendpunkt – war im Acalabrutinib-Arm noch nicht erreicht, während es im IdR/BR-Arm 16,5 Monate betrug. Das relative Risiko für Krankheitsprogression oder Tod konnte mit dem BTKi im Vergleich zu IdR/BR um 69 % gesenkt werden.4
Neben der starken Wirksamkeit belegte die primäre Auswertung der ASCEND-Studie auch die gute Verträglichkeit von Acalabrutinib. So waren im Unterschied zu IdR bzw. BR kaum Dosisreduktionen erforderlich und deutlich weniger Therapieabbrüche aufgrund von unerwünschten Ereignissen zu verzeichnen.4
3-Jahres-Update bestätigt anhaltende Wirksamkeit
Im Dezember 2021 wurde bei der Jahrestagung der American Society of Hematology (ASH) in Atlanta (USA) das 3-Jahres-Update der ASCEND-Studie von Prof. Wojciech Jurczak (Krakau, Polen) präsentiert.5 Auch in der Langzeit-Nachbeobachtung blieb die Wirksamkeit der Acalabrutinib-Monotherapie erhalten und zeigte einen signifikanten PFS-Vorteil im Vergleich mit den Standardtherapieschemata bei Patient:innen mit R/R-CLL (s. Abb. 2 und 3):5,6
- 71 %ige Risikoreduktion für Krankheitsprogression oder Tod mit Acalabrutinib vs. IdR/BR;
- 63 % PFS nach einer medianen Nachbeobachtungszeit von 36 Monaten unter Acalabrutinib vs. 21 % PFS unter IdR/BR nach median 35,2 Monaten;
- medianes PFS unter Acalabrutinib nicht erreicht vs. 16,8 Monate unter IdR/BR;
- niedrige Raten an kardiovaskulären Ereignissen aller Grade unter der Therapie mit dem Acalabrutinib (Vorhofflimmern: 7 %; Bluthochdruck: 7 %).
Acalabrutinib: überzeugender PFS-Vorteil im Rezidiv auch nach 3jähriger Behandlungsdauer – in allen relevanten Subgruppen mit genetischen Hochrisikomerkmalen
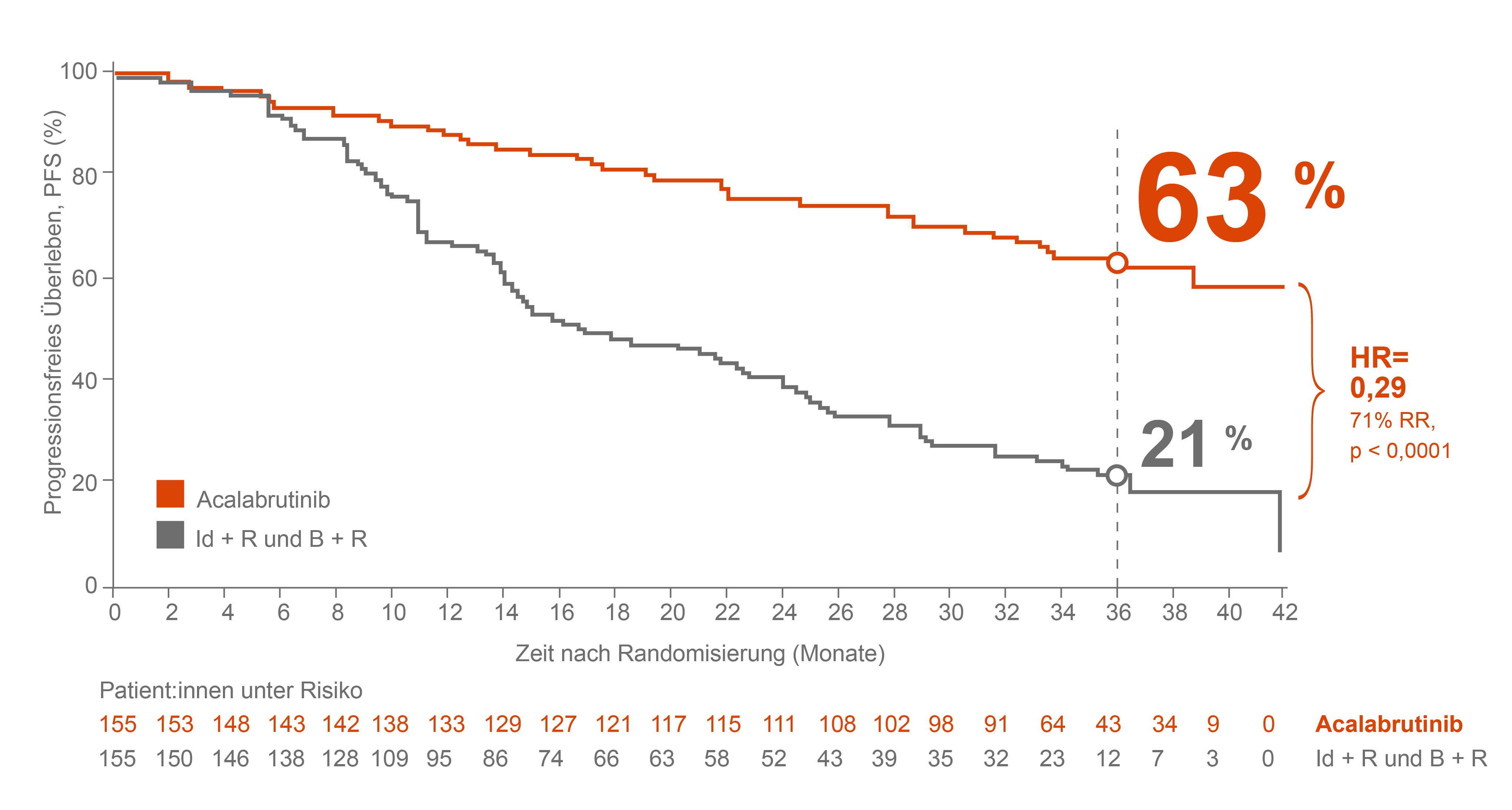
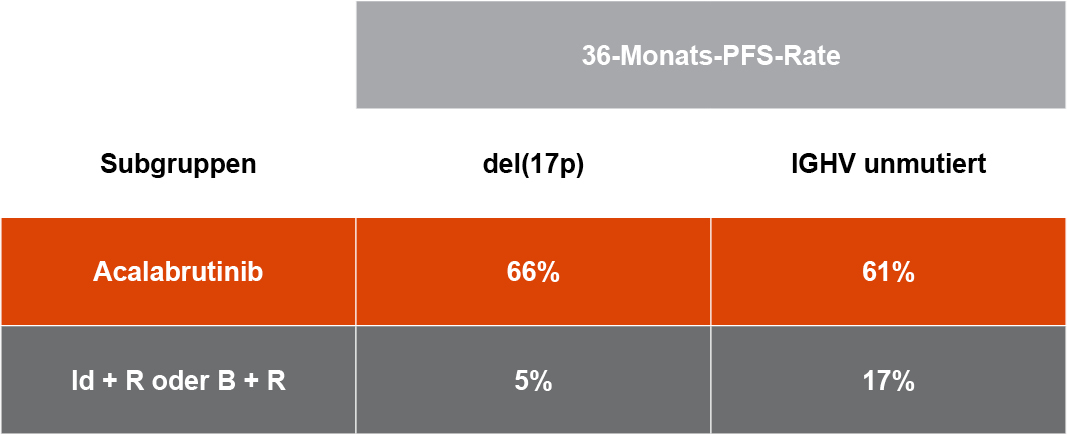
Abbildung adaptiert nach Jurczak et al 20215 B + R = Bendamustin + Rituximab; HR = Hazard Ratio; Id + R = Idelalisib + Rituximab; PFS = progressionsfreies Überleben; RR = Risikoreduktion
Das mediane Gesamtüberleben (OS) war in beiden Gruppen noch nicht erreicht. Die 36-Monats-OS-Rate betrug für Acalabrutinib 80 % versus 73 % für IdR/BR. In diesem Zusammenhang wies Jurczak darauf hin, „dass beinahe 50 % der Patient:innen aus dem Vergleichsarm in den Acalabrutinib-Arm wechselten, was die Möglichkeiten der Studie zum Aufdecken von Unterschieden beim Gesamtüberleben einschränken dürfte.“7
Vorteile bezüglich Wirksamkeit und Nutzen-Risiko-Profil
Trotz der längeren Behandlungsexposition brachen weniger Patienten unter Acalabrutinib als im Vergleichsarm (n = 83; 65 % unter IdR bzw. 17 % unter BR) die Therapie vorzeitig wegen unerwünschter Ereignisse ab (Acalabrutinib: 21 %; IdR bzw. BR: 54 %).5 Der BTKi wies damit wie in der Primäranalyse nicht nur bezüglich der Wirksamkeit, sondern auch hinsichtlich der Sicherheit Vorteile gegenüber den Standard-Therapieregimes auf. Im Rahmen der längeren Nachbeobachtung waren jenseits des bekannten Verträglichkeitsprofils von Acalabrutinib keine neuen Sicherheitssignale zu beobachten.5,6 „Die Behandlungsexposition wurde unter Acalabrutinib im Vergleich mit dem anderen Therapiearm als gut betrachtet“, betonte Jurczak.7
Eine Post-hoc-Risiko-Nutzen-Analyse8, die ebenfalls beim ASH 2021 präsentiert wurde, bestätigt diese Einschätzung. In die Untersuchung wurden neben der ASCEND-Studie auch Daten aus der ELEVATE RR-Studie einbezogen, dem ersten direkten BTKi-Vergleich zwischen Acalabrutinib und Ibrutinib.9 Die integrierte Betrachtung von Wirksamkeit, Sicherheit und Lebensqualität (Q-TWiST-Analyse) belegt für die R/R-CLL-Therapiesituation eine signifikante Überlegenheit von Acalabrutinib gegenüber der IdR/BR-Behandlung und – variierend je nach Definition der Toxizität – numerische Vorteile gegenüber Ibrutinib hinsichtlich des qualitätsadjustierten Überlebens.8
Profunde Evidenzbasis für Acalabrutinib als Therapie bei CLL
Die Ergebnisse der ELEVATE-RR-Studie9,10 wurden der Fachöffentlichkeit im Juni des vergangenen Jahres beim ASCO 2021 vorgestellt, zeitgleich mit dem 4-Jahres-Update der ELEVATE TN-Studie11,12. In nur einem Jahr hat sich Acalabrutinib als Option für eine optimierte CLL-Therapie sowohl in der Erstlinie als auch bei Rezidiv und Refraktärität etabliert. Die überzeugenden Langzeitdaten der Zulassungsstudien, der direkte Head-to-Head-Vergleich mit Ibrutinib und die Ergebnisse indirekter Vergleichsuntersuchungen untermauern den Stellenwert von Acalabrutinib in der gegenwärtigen CLL-Therapielandschaft.
Quellen
- Wendtner CM et al. Onkopedia-Leitlinie Chronische Lymphatische Leukämie (CLL). Stand: September 2020
- Fachinformation Calquence®, aktueller Stand
- Sharman JP et al. Acalabrutinib with or without obinutuzumab versus chlorambucil and obinutuzmab for treatment-naive chronic lymphocytic leukaemia (ELEVATE TN): a randomised, controlled, phase 3 trial. Lancet 2020;395(10232):1278-91
- Ghia P et al. ASCEND: Phase III, Randomized Trial of Acalabrutinib Versus Idelalisib Plus Rituximab or Bendamustine Plus Rituximab in Relapsed or Refractory Chronic Lymphocytic Leukemia. J Clin Oncol 2020;38(25):2849-61
- Jurczak W et al. Presentation at: ASH; December 11–14, 2021; Atlanta, Georgia
- Jurczak W et al. Acalabrutinib vs Rituximab plus Idelalisib or Bendamustine in Relapsed/Refractory Chronic Lymphocytic Leukemia: A Three-Year Follow-Up of the ASCEND Trial. Blood 2021;138(Suppl_1):393
- Dobkowski D. Acalabrutinib Provides Long-Term Survival Benefits Vs. Standard of Care in Relapsed/Refractory Chronic Lymphocytic Leukemia. OncLive; December 12, 2021 (onclive.com; Zugriff am 10.01.2022)
- Seymour JF et al. A quality-adjusted survival (Q-TWiST) analysis to assess benefit-risk of acalabrutinib versus idelalisib/bendamustine plus rituximab or ibrutinib among relapsed/refractory (R/R) chronic lymphocytic leukemia (CLL) patients. Blood 2021;138(Suppl_1):3722
- Byrd JC et al. Acalabrutinib Versus Ibrutinib in Previously Treated Chronic Lymphocytic Leukemia: Results of the First Randomized Phase III Trial. J Clin Oncol 2021;39:3441-52
- Byrd JC et al. J Clin Oncol 2021; 39 (suppl 15; abstr 7500). DOI: 10.1200/JCO.2021.39.15_suppl.7500
- Sharman JP et al. Efficacy and safety in a 4-year follow-up of the ELEVATE-TN study comparing acalabrutinib with or without obinutuzumab versus obinutuzumab plus chlorambucil in treatment-naïve chronic lymphocytic leukemia Leukemia 2022. https://doi.org/10.1038/s41375-021-01485-x (letzter Abruf: 18.01.2022)
- Sharman JP et al. J Clin Oncol 2021;39(suppl_15):7509. DOI: 10.1200/JCO.2021.39.15_suppl.7509
Abkürzungen:
ASCO = American Society of Clinical Oncology (bzw. deren Jahreskongress)
ASH = American Society of Hematology (bzw. deren Jahreskongress)
BCL-2 = B-Zell-Lymphom-2 (Protein)
BR = Bendamustin plus Rituximab
BTK = Bruton-Tyrosinkinase
BTKi = Bruton-Tyrosinkinase-Inhibitor
ECOG = Eastern Cooperative Oncology Group
EMA = Europäische Arzneimittel-Agentur (European Medicines Agency)
HR = Hazard Ratio
IdR = Idelalisib plus Rituximab
IGHV = variable Regionen der schweren Ketten der Immunglobuline
IRC = independent review committee
KI = Konfidenzintervall
PS = Performance Status
Q-TWiST = Quality-adjusted Time Without Symptoms and Toxicity