Neuer Therapiestandard bei CLL: Acalabrutinib im Praxiseinsatz
Acalabrutinib ist ein neuer leitliniengerechter Standard für die Behandlung von Patienten mit chronischer lymphatischer Leukämie – in allen Indikationssegmenten, wie drei typische Fallbeispiele aus der Praxis verdeutlichen.
Der Bruton-Tyrosinkinase-Inhibitor (BTKi) Acalabrutinib (Calquence®) ist in Europa seit November 2020 für die Behandlung von therapienaiven oder vorbehandelten Patienten mit chronischer lymphatischer Leukämie (CLL) zugelassen.1 In der Erstlinie besteht neben der Anwendung als Monotherapie auch die Option zur Kombination mit dem Anti-CD20-Antikörper Obinutuzumab.1,2
Vor der Zulassung des Zweitgenerations-BTKi Acalabrutinib war Ibrutinib als einzig verfügbarer BTKi jahrelang im Einsatz und konnte seine gute Wirksamkeit demonstrieren. Allerdings wirkt sich das Toxizitätsprofil dieses BTKi der ersten Generation im realen Versorgungsalltag teilweise therapielimitierend aus. Bei einigen Patienten sind Dosisreduktionen, Therapieunterbrechungen oder - laut einer größeren Real-World Analyse bei fast jedem vierten patienten - der vollständige Abbruch der Ibrutinib-Therapie erforderlich.3-6 Dafür werden zumindest teilweise Off-Target-Effekte verantwortlich gemacht, da Ibrutinib neben der BTK auch die Aktivität mehrerer anderer Kinasen relevant beeinträchtigt.7-9
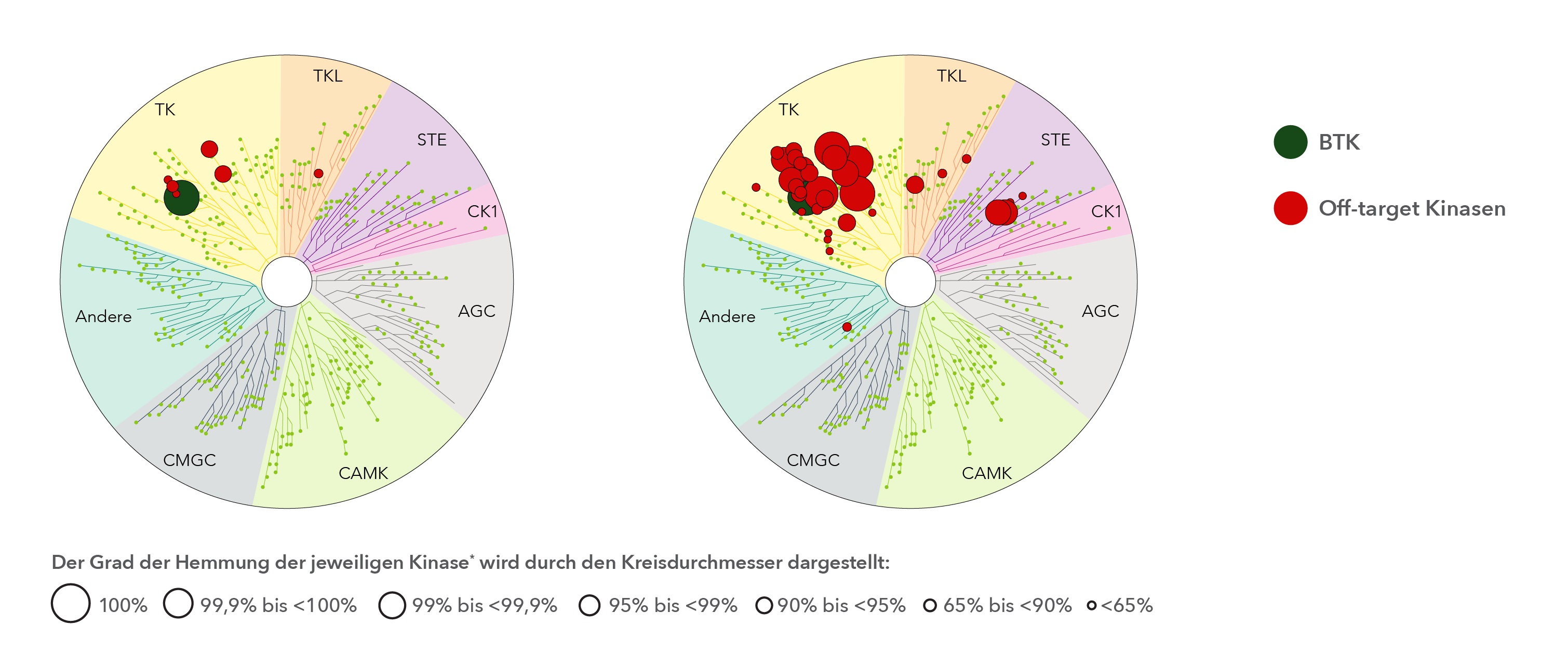
Abb. 1: Ergebnisse aus In-vitro-Untersuchungen zur Kinasehemmung bei Acalabrutinib und Ibrutinib. (adaptiert nach Herman SEM et al. 2017)8
Optimierte Selektivität zur medizinischen Bedarfsdeckung
Um den medizinischen Bedarf nach einem neuen, verträglicheren BTKi zu decken, wurde Acalabrutinib mit dem Ziel einer optimierten Selektivität entwickelt.10 Wie In-vitro-Analysen zeigten, hemmt Acalabrutinib tatsächlich fast ausschließlich die BTK, was ein verändertes und günstigeres Verträglichkeitsprofil gegenüber Ibrutinib erwarten lässt.7,8 Klinische Vorteile zugunsten von Acalabrutinib konnten – zusammen mit einer vergleichbaren Wirksamkeit – in der Studie ELEVATE RR bei vorbehandelten CLL-Patienten bestätigt werden.11 Die ersten Ergebnisse dieses randomisierten Head-to-Head-Vergleichs mit Ibrutinib wurden beim ASCO 2021 ebenso präsentiert wie das 4-Jahres-Update der Studie ELEVATE TN.12
Die aktuelle Auswertung der zulassungsrelevanten Phase-III-Studie ELEVANTE TN bestätigt auch über diesen längeren Beobachtungszeitraum die überlegene Wirksamkeit sowie das konsistente Sicherheitsprofil von Acalabrutinib als Monotherapie und in Kombination mit Obinutuzmab bei therapienaiven Patienten im Vergleich zur Chemoimmuntherapie mit Chlorambucil und Obinutuzumab.12
In mehreren indirekten Vergleichsanalysen zeichnen sich zudem Vorteile der Acalabrutinib-basierten Therapien im Vergleich zu anderen zielgerichteten Regimen in der Erstlinie ab – insbesondere im Sinne eines niedrigeren Nebenwirkungsrisikos ohne Wirksamkeitsverlust.13-16
Acalabrutinib: ein neuer Leitlinien-Standard in allen Therapiesegmenten
Wie den Therapiealgorithmen der im September 2020 aktualisierten Onkopedia-Leitlinie zur CLL zu entnehmen ist, wird der Einsatz von Acalabrutinib für therapiebedürftige Patienten in allen Indikationssegmenten empfohlen.2 Letztlich hängt die individuelle Therapieentscheidung maßgeblich von den Risikofaktoren, der körperlichen Fitness, der Lebenssituation, den Präferenzen des Patienten und im Falle einer rezidivierenden bzw. refraktären CLL von der Vorbehandlung ab.2
Drei typische Fallbeispiele aus dem Behandlungsalltag, die kürzlich in einem Praxisreport publiziert wurden17, verdeutlichen das nahezu uneingeschränkte Einsatzspektrum von Acalabrutinib:
a) Unvorbehandelte CLL-Patientin (68 Jahre) im Stadium Binet C:
- 68-jährige Frau:
- Komorbiditäten: Hyperthyreose, arterielle Hypertonie, Diabetes mellitus;
- Medikation: Ranitidin, Metoprolol, Metformin, Simvastatin.
- 03/2019: Diagnose einer CLL im Stadium Binet A bei Vorstellung zur Routineuntersuchung beim Hausarzt:
- Labor: Lymphozyten 23,7/nl; Hb 11,1 g/dl; Thrombozyten 112/nl;
- zunächst keine CLL-Therapie.
- 10/2020: Einstufung in Stadium Binet C:
- deutlicher Leistungsabfall berichtet;
- ECOG PS 0 („Go-go“-Patientin);
- Labor: Hb 9,3 g/dl; Thrombozyten 78/nl;
- unmutierter IGHV-Mutationsstatus (keine weiteren genetischen Risikofaktoren
- gemäß CLL-IPI: Hochrisiko-CLL (Alter > 65 Jahre; Binet C; Beta-2-Mikroglobulin > 3,5 mg/l; unmutierter IGHV-Status) mit einer geschätzten Wahrscheinlichkeit für das 5-Jahres-Überleben von 63,6 %.
- Therapiewahl mittels Risikostratifizierung:
- keine Chemoimmuntherapie aufgrund der Überlegenheit der zielgerichteten Substanzen;
- keine Therapie mit einem Anti-CD20-Antikörper vor dem Hintergrund der COVID-19-Situation (Gefahr einer verminderten Impfantwort durch B-Zell-Depletion, Infusionspflichtigkeit, häufige Praxisbesuche);
- oraler BTKi: bevorzugte Wahl von Acalabrutinib aufgrund des günstigeren Risiko-Nutzen-Profils angesichts der Begleiterkrankungen und -medikation (arterielle Hypertonie und erhöhtes Risiko für Vorhofflimmern; s. o.) .
(Fallbeispiel von Dr. Ingo Schwaner, Berlin)17
b) Mehrfach vorbehandelter CLL-Patient:
- 72-jähriger Mann.
- Komorbiditäten:
- insulinpflichtiger Diabetes mellitus Typ 1, sensomotorische Polyneuropathie, arterielle Hypertonie, Hyperurikämie;
- kompensierte Niereninsuffizienz (Z. n. akutem Nierenversagen im Rahmen eines fieberhaften Infekts 04/2019);
- 08/2019: koronare 3-Gefäßerkrankung (Z. n. Myokardinfarkt und erfolgreicher Rekanalisation mit DE-Stent);
- Medikation: ASS 100 mg; Bisoprolol 2,5 mg; Candesartan 2 × 16 mg; Amlodipin 2 × 5 mg; Atorvastatin 80 mg; L-Thyroxin 50 µg; Allopurinol 150 mg; Insulin aspart sowie Insulin glargin.
- 03/2009: CLL-Erstdiagnose im Rahmen einer Lymphozytose-Abklärung:
- Stadium Binet A, unmutierter IGVH-Status, del13q-Mutation;
- regelmäßige Kontrollen in Abständen von 3–6 Monaten.
- 07/2012: Autoimmunhämolytische Anämie:
- Leukozyten 27,8/nl; Hb 5,6 g/dl; Thrombozyten 61/nl); generalisierte Lymphadenopathie (Größe der einzelnen Herde bis max. 4 cm; Milzgröße: 16 x 5 cm);
- erneute zytogenetische Diagnostik: del13q- und del6q-Mutation;
- 07–09/2012: Therapie mit Prednisolon und Cyclophosphamid => Sistieren der autoimmunhämolytischen Anämie.
- 09/2012–02/2013: Erste CLL-Therapie mit Bendamustin + Rituximab:
- sehr gute partielle Remission;
- regelmäßige Kontrollen in Abständen von 3–6 Monaten;
- ab 10/2016: langsame Progredienz.
- 07/2018: Erneute Therapiebedürftigkeit wegen zunehmender B-Symptomatik:
- Leukozyten 123/nl; Hb 11,7 g/dl; Thrombozyten 125/nl; generalisierte Lymphadenopathie (bis max. 3 cm; Milzgröße: 17 × 6 cm);
- del13q- und del6q-Mutation, TP53-Wildtyp;
- Therapie mit Ibrutinib empfohlen, aber Patientenpräferenz für zeitlich begrenzte Therapie; wegen zuvor gutem Ansprechen und langer therapiefreier Zeit deshalb erneut 6 Zyklen Bendamustin + Rituximab => sehr gute partielle Remission.
- Schnelle Progredienz der CLL (seit 04/2020) und erneute Therapiebedürftigkeit (08/2020):
- Leukozyten 29,5/nl; Hb 9,6 g/dl; Thrombozyten 206/nl; generalisierte Lymphadenopathie (bis max. 2 cm; Milzgröße 14 × 5,5 cm);
- B-Symptomatik mit Nachtschweiß, Gewichtsverlust von 5 kg, Leistungsknick;
- ECOG PS 1;
- del13q- und del6q-Mutation; neu: TP53-Mutation C415T in Exon 5;
- 10/2020: CLL-Therapie mit Acalabrutinib (2 × 100 mg; Behandlungsbeginn im Rahmen einer Studie):
- therapiebedingt zunächst Leukozyten-Anstieg bis auf max. 97/nl in Woche 7 nach Therapiebeginn;
- 12/2020: fieberhafte Bronchitis: im HR-CT konfluierende Infiltrate im linken Lungenunterlappen (Pneumonie bei Immunglobulinmangel), mehrfach negativer SARS-CoV-2-Abstrich (PCR) => Abklingen nach Substitutionsbehandlung mit polyklonalem Immunglobulin und antibiotischer Therapie;
- nach 6-monatiger Behandlungsdauer unter fortgesetzter Acalabrutinib-Therapie:
- deutliche Verbesserung des Allgemeinbefindens (keine B-Symptomatik mehr; ECOG PS 0; Gewichtszunahme um 5 kg);
- Leukozyten 25,8/nl, Hb 11 g/dl; Thrombozytenzahl 172/nl;
- sehr gute Verträglichkeit von Acalabrutinib im weiteren Verlauf; trotz bekannter kardiovaskulärer Risikofaktoren (s. o.) keine Hinweise für unerwünschte kardiale Ereignisse wie z. B. Vorhofflimmern.
- Stand Juli 2020: Fortführung der Behandlung mit Acalabrutinib und der Immunglobulin-Substitution.
(Fallbeispiel von Dr. Burkhard Schmidt, München)17
c) Therapieumstellung bei kardialer Problematik unter Ibrutinib:
- 78-jähriger Mann.
- Keine relevante Komorbidität, Patient noch sehr sportlich (Rennradfahrer).
- 04/2020: Diagnose einer CLL im Stadium Binet C:
- Leukozytenzahl 195/nl;
- symptomatische, transfusionspflichtige Anämie (normozytär, normochrom, hyporegenerativ; Hb initial 5,9 mg/dl; negativer Coombs-Test);
- erhebliche Knochenmarkinfiltration mit CLL-Zellen (mehr als 80 %);
- unmutierter IGHV-Status, 11q-Mutation.
- CLL-Erstlinientherapie mit BTKi (Ibrutinib):
- komplette Remission mit Normalisierung des Blutbilds;
- CLL-Zellen nur noch in der Immunzytologie nachweisbar
- monatliche Verlaufskontrollen;
- Wiederaufnahme der sportlichen Aktivität bei sehr gutem Allgemeinbefinden.
- 10/2020: Vorstellung wegen neu aufgetretener Belastungsdyspnoe:
- Arrhythmie mit Vorhofflimmern;
- unter eingeleiteter Antikoagulation (Edoxaban 60 mg) Entwicklung einer ausgeprägten Hämatomneigung.
- 12/2020: Umstellung auf Acalabrutinib:
- 01/2021: bei nächster Kontrolle anhaltende Remission hinsichtlich der CLL sowie Sistieren des Vorhofflimmerns => Antikoagulation beendet;
- 02/2021: bei letzter verfügbarer Untersuchung weiterhin sehr gutes Befinden; kein erneutes Auftreten von Vorhofflimmern oder Hämatomen; vollumfängliche Wiederaufnahme der sportlichen Aktivitäten.
(Fallbeispiel von Prof. Philipp Staber, Universitätsklinik für Innere Medizin, Wien)17
- Fachinformation Calquence®, Stand: November 2020
- Wendtner CM et al. Onkopedia-Leitlinie Chronische Lymphatische Leukämie (CLL). Stand: September 2020
- Mato AR et al. Toxicities and outcomes of 616 ibrutinib-treated patients in the United States: a real-world analysis. Haematologica 2018;103(5):874-9
- Hou J. Dose reductions and discontinuations with chronic lymphocytic leukemia (CLL) patients receiving ibrutinib in community and academic settings. Blood 2020;136 (Suppl_1):12-3
- Nuttall E et al. Real-world experience of ibrutinib therapy in relapsed chronic lymphocytic leukemia: results of a single-center retrospective analysis. J Blood Med 2019;10:199-208
- Hampel PJ et al. Rapid disease progression following discontinuation of ibrutinib in patients with chronic lymphocytic leukemia treated in routine clinical practice. Leuk Lymphoma 2019;60(11):2712-9
- Barf T et al. Acalabrutinib (ACP-196): A Covalent Bruton Tyrosine Kinase Inhibitor with a Differentiated Selectivity and In Vivo Potency Profile. J Pharmacol Exp Ther 2017;363(2):240-52
- Herman SEM et al. The Bruton’s tyrosine kinase (BTK) inhibitor acalabrutinib demonstrates potent on-target effects and efficacy in two mouse models of chronic lymphocytic leukemia. Clin Cancer Res 2017;23(11):2831-41
- Xiao L et al. Ibrutinib-Mediated Atrial Fibrillation Attributable to Inhibition of C-Terminal Src Kinase. Circulation 2020;142(25):2443-55
- Harrington BK et al. ACP-196 Is a Second Generation Inhibitor of Bruton Tyrosine Kinase (BTK) with Enhanced Target Specificity. Blood 2015;126(23):2908
- Byrd JC et al. First results of a Head-to-Head trial of acalabrutinib versus ibrutinib in previously treated chronic lymphocytic leukemia. J Clin Oncol 2021;JCO2101210. doi:10.1200/JCO.21.01210
- Sharman JP et al. Acalabrutinib ± obinutuzumab vs obinutuzumab + chlorambucil in treatment-naïve chronic lymphocytic leukemia: ELEVATE-TN 4-year follow-up. J Clin Oncol 2021;39(suppl_15):7509
- Sheng Z et al. Comparison of acalabrutinib plus obinutuzumab, ibrutinib plus obinutuzumab and venetoclax plus obinutuzumab for untreated CLL: a network meta-analysis. Leuk Lymphoma 2020;61(14):3432-9
- Messori A, Bartoli L. Restricted mean survival time in patients with chronic lymphocytic leukemia treated with chemotherapy-free regimens as first line. Leuk Lymphoma 2021;62(4):1018
- Davids MS et al. Comparative Efficacy of Acalabrutinib in Frontline Treatment of Chronic Lymphocytic Leukemia: A Systematic Review and Network Meta-analysis. Clin Ther 2020;42(10):1955-74.e15
- Davids MS et al. Matching-adjusted indirect comparisons of safety and efficacy of acalabrutinib versus other targeted therapies in patients with treatment-naïve chronic lymphocytic leukemia. Leuk Lymphoma 2021;1-16. doi:10.1080/10428194.2021.1913144
- Hoechstetter M, Staber P. Calquence® bei chronischer lymphatischer Leukämie (CLL). Thieme Praxis Report, Oktober 2021:1-16
Abkürzungen:
AGC = Zusammenfassung der Proteinkinasen A, G und C
BTK = Bruton-Tyrosinkinase
CAMK = Calmodulin-abhängige Kinasen
CK1 = Caseinkinase 1
CMGC = Zusammenfassung von CDK (Cyclin-abhängige Kinasen)
MAPK (Mitogen-aktivierte Proteinkinasen)
GSK3 (Glykogensynthase-Kinase 3 und ähnliche Kinasen)
CLK (CDK-ähnliche Kinasen)
TK = Tyrosinkinasen
TKL = Tyrosinkinase-ähnliche Kinasen
STE = Kinasen mit Ähnlichkeit zu Steril-7, -11 und -20 aus Saccharomyces cerevisiae
* Profil von CALQUENCE® und Ibrutinib in einem kompetitiven Bindungstest mit 395 menschlichen Kinasen und krankheitsrelevanten Mutanten, bei Testung einer Konzentration von 1 μM im Vergleich zu unbehandelter Kontrolle. [Quellen-Verweis]
DE-39985/21
