- Tainsky MA. Biochim Biophys Acta. 2009;1796:176-193.
- https://www.onkopedia.com/de/onkopedia/guidelines/chronische-lymphatische-leukaemie-cll/@@guideline/html/index.html. Stand September 2020. (letzter Abruf: 05.11.2020).
- The International CLL-IPI working group. Lancet Oncol. 2016;17:779-790.
- Von Tresckow J et al. Dtsch Arztebl Int. 2019;116:41-46.
- Leitlinienprogramm Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF):S3-Leitlinie zur Diagnostik, Therapie und Nachsorge für Patienten mit einer chronischen lymphatischen Leukämie(CLL), Langversion 1.0, 2018,AWMF Register-nummer: 018-032OL, http://www.leitlinienprogramm-onkologie.de/leitlinien/chroni-sche-lymphatische-leukaemie-cll/ (letzter Abruf: 05.11.2020).
- Mia R et al. Cancers. 2020;12:642:doi:10.3390/cancers12030642.
- Cohen JA et al. Cancers. 2020,12,894;doi:10.3390/cancers12040894.
- Rosati E et al. Front Oncol. 2018;8:229.
- Del Giudice I et al. Haematologica. 2012;97; https://doi.org/10.3324/haematol.2011.060129 (letzter Abruf: 05.11.2020).
- Zhang Z et al. Oncotarget. 2017;8:69916-69923.
- Lee J und Wang YL. J Mol Diagn. 2020;22:1114-1125.
Biomarker: Lotsen für die CLL-Therapie
Biomarker können für die Früherkennung, Diagnose, Prognose und Vorhersage des Ansprechens auf die Behandlung sowie das Wiederauftreten der Erkrankung herangezogen werden.<sup>1</sup> Bei chronischer lymphatischer Leukämie (CLL) sind verschiedene prognostische Parameter bekannt und weitere in der Validierung.
Um die Prognose vor Einleitung einer Erstlinientherapie besser abzuschätzen und den individuellen Krankheitsverlauf besser vorherzusagen, kann der CLL International Prognostic Index (IPI) bestimmt werden.2,3 Er teilt Patienten in vier Risikogruppen ein. Zur Berechnung sind folgende Parameter erforderlich (siehe Tabelle).3,4
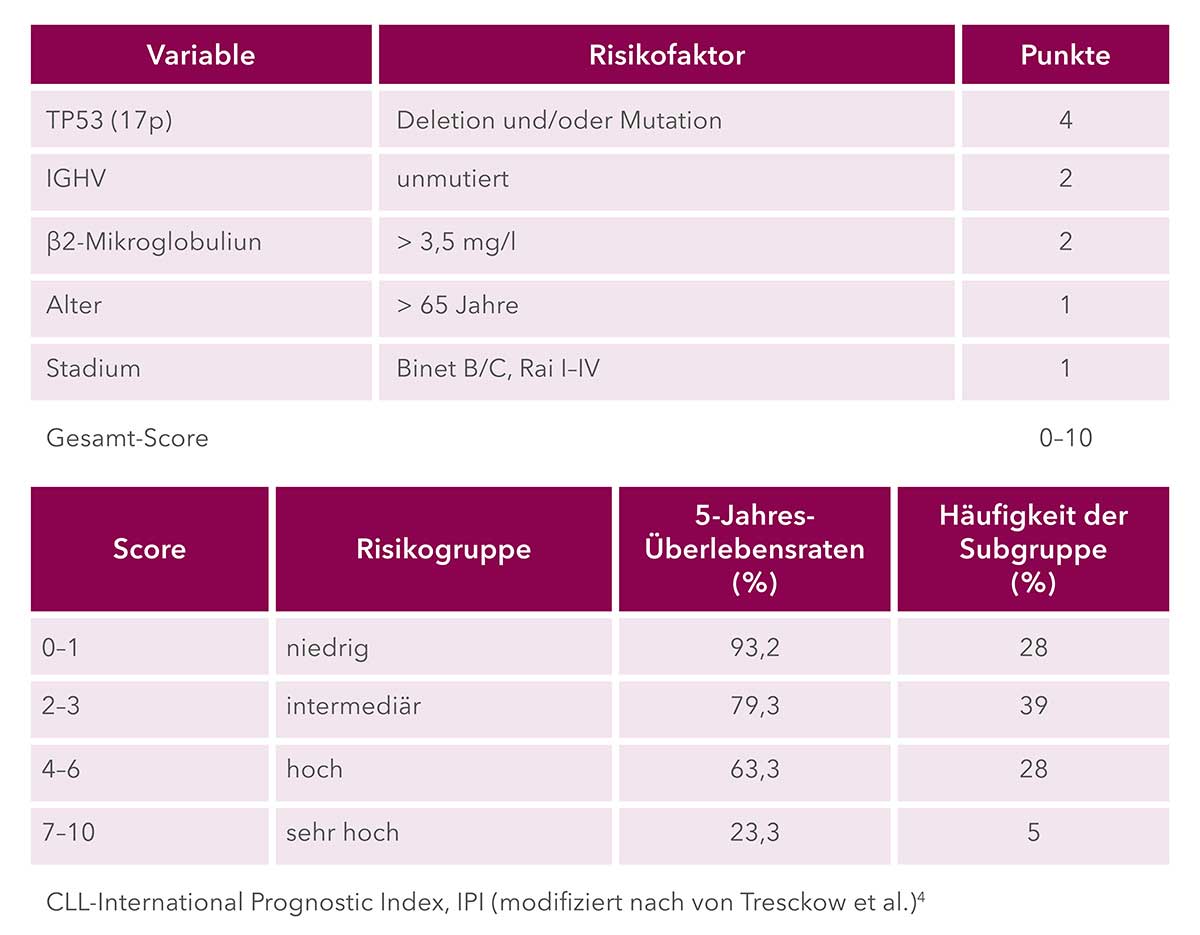
Dieser prognostische Index wurde allerdings nicht auf Basis neuer zielgerichteter Therapien validiert.2 Zudem besitzt die Einteilung der Patienten in die verschiedenen Risikogruppen bislang keine klinische Konsequenz. Daher wird empfohlen, den IPI nur in klinisch relevanten Fällen und/oder bei Therapiebedürftigkeit zu bestimmen. Bei noch nicht behandlungsbedürftigen Patientinnen und Patienten sollte vermieden werden, durch einen ungünstigen Prognose-Score weitere Verunsicherung hervorzurufen.5
Im Sinne einer Präzisionsmedizin kann die Einbeziehung molekularer Biomarker entscheidend zur Therapiewahl bei CLL beitragen.6 Der TP53-Status, eine Deletion auf Chromosom 17 (del(17p)), ein komplexer Karyotyp und der IGHV-Mutationsstatus sind die wichtigsten Parameter für die Wahl der Erstlinientherapie.2 TP53-Mutationen, del(17p), unmutiertes IGHV und ein komplexer Karyotyp sind mit einer niedrigen Ansprechrate und kürzerem progressionsfreien Überleben (PFS) und Gesamtüberleben nach Chemotherapie und Chemoimmuntherapie verbunden – daher empfiehlt die aktuelle Onkopedia-Leitlinie als Erstlinientherapie den Einsatz von BTKi oder alternativ der Kombination aus Venetoclax plus Obinutuzumab.2
Die Entdeckung von Biomarkern hat die Prognose und Vorhersage des Therapieansprechens bei CLL revolutioniert. Dennoch bleibt ihr genauer hierarchischer Wert fraglich, insbesondere in Zeiten zielgerichteter Therapieoptionen.7
Die aktuelle Onkopedia-Leitlinie empfiehlt vor Einleitung einer Therapie eine TP53-Mutationsanalyse; eine Testung auf IGHV-Mutationen sowie eine zytogenetische Untersuchung auf 17p-Deletionen und komplexen Karyotyp sowie weitere genetische Untersuchungen bei atypischem Phänotyp zur Abgrenzung gegenüber anderen indolenten Lymphomen.2
Molekulargenetische Untersuchungen tragen zunehmend zur Aufklärung der CLL-Pathogenese bei. Proteine, die die Veränderung des Metabolismus, der Zellteilung und der antiapoptotischen Mechanismen von B-Zellen beeinflussen, sind potenzielle Biomarker bei der CLL:
- NOTCH1: NOTCH1 ist eines der häufigsten in CLL-Zellen mutierten Gene bei Diagnose. Mutationen im NOTCH1-Gen weisen auf einen schlechten Therapieverlauf und schwer zu behandelnde CLL hin.8 Dies ist insbesondere bei CLL-Patienten mit Trisomie 12 und nichtmutierten IGHV-Genen der Fall.9
- SF3B1: Untersuchungen sprechen für eine Rolle von Mutationen im SF3B1-Gen als prognostischer Faktor für das PFS und OS bei CLLPatienten.10
- BIRC3: BIRC3 ist ein negativer Regulator des NF kB-Signalwegs. BIRC3-Mutationen sind in etwa 4 % aller Fälle von CLL nachweisbar. Während eine Studie BIRC3-Mutationen mit Hochrisiko-CLL assoziierte, konnten andere Studien die prognostische Signifikanz nicht bestätigen.11
- ATM: Die Serin/Threonin-Kinase ATM ist ein zentraler Regulator der DNA-Reparatur. ATM-Mutationen sind in etwa 12 % aller Fälle von CLL nachweisbar. Die Assoziation mit einer schlechten Prognose der CLL wird kontrovers diskutiert.11
Die Autoren der Onkopedia-Leitlinie betonen, dass potenzielle biologische Prognosefaktoren wie die genannten, sowie weitere genetische Veränderungen weiterhin der prospektiven Validierung bedürfen. Sie sind derzeit nicht Grundlage spezifischer, therapeutischer Überlegungen. Ihre routinemäßige Bestimmung ist außerhalb klinischer Studien bisher noch nicht indiziert.2