Eine 77-jährige Frau, die bis auf eine mit 69 Jahren diagnostizierte Asthmaerkrankung zuvor bei guter Gesundheit war, stellte sich im Oktober mit seit 7–10 Tagen fortschreitend zunehmender Dyspnoe (NYHA II bis IV) in der Notaufnahme vor. Die Patientin verneinte Fieber, Husten, Auswurf, Brustschmerzen oder Hämoptyse. Sie verneinte ähnliche Episoden in der Vergangenheit. Sie verneinte auch, derzeit oder in der Vergangenheit geraucht zu haben. In ihrer früheren Krankengeschichte berichtete die Patientin von absolutem Wohlbefinden bis zum Alter von 69 Jahren, als bei ihr Asthma bronchiale diagnostiziert wurde. Dann erfolgte die Diagnose eines Asthma bronchiale mit erfolgreicher bronchodilatatorischer Therapie.
Vor einem Monat wurde die Patientin aus der pulmonologischen Abteilung mit der Diagnose einer Ateminsuffizienz aufgrund einer beidseitigen interstitiellen Pneumonie, verursacht durch Chlamydia pneumoniae, und einer Verschlimmerung des Asthmas entlassen. Bei dieser Gelegenheit wurde eine Dünnschicht-CT-Untersuchung des Brustkorbs durchgeführt, die das Vorhandensein mehrerer unscharfer Bereiche mit einem milchglasartigen Erscheinungsbild auf beiden Seiten dokumentierte. Darüber hinaus hatte sich eine Anämie mit Hämoglobinwerten von 8,2 g/dl und einem MCV von 84 fl entwickelt, für die eine Bluttransfusion indiziert war, die die Patientin jedoch aus religiösen Gründen (Zeugin Jehovas) abgelehnt hatte.
Dies sind die Ergebnisse der Laboruntersuchungen:
- WBC – N/µl 19920
- Neutrophile – N/µl 14400
- Lymphozyten – N/µl 2300
- Eosinophile – N/µl 2000
- Hb – g/dl 6,7
- MCV – fl 80
- CRP – mg/dl 8,5
- Na – mEq/l 140
- K – mEq/l 3,7
- Kreatinin – mg/dl 1,01
Es wird auch eine arterielle Blutgasanalyse in Umgebungsluft durchgeführt, die das Vorliegen einer respiratorischen Insuffizienz vom Typ 1 dokumentiert:
- pH 7,53
- pCO2 34,9 mmHg
- pO2 44,7 mmHg
- SO2 84,5 %
- HCO3 29,5 mmol/l
Es wird eine Röntgenaufnahme des Brustkorbs angefertigt. Das Bild zeigt eine interstitielle Verdickung auf bibasaler Höhe, in deren Zusammenhang eine unscharfe Verdickung an der Basis der rechten Lunge zu erkennen ist.

Aufnahme in die Abteilung für Innere Medizin
Nach Beurteilung ihres klinischen Zustands wurde die Patientin mit der Diagnose Anämie und Ateminsuffizienz mit rechtsseitiger basaler Lungenkonsolidierung in die Abteilung für Innere Medizin aufgenommen. Bei der Aufnahme in die Abteilung war die Patientin wach, klar und kooperativ; Blutdruck 140/80 mmHg, Herzfrequenz 110 Schläge pro Minute, rhythmisch, Atemfrequenz 32 Atemzüge pro Minute; SpO2 94 % mit Venturi-Maske 35 % 8 l/min. Haut und Schleimhäute blass; kein Hautausschlag.
Brustkorb: diffuse verminderte Atemgeräusche mit vereinzelten pfeifenden Atemgeräuschen und Rasselgeräuschen an der rechten Basis; Herzgeräusche gültig und rhythmisch, tachykardisch, ohne Pausen. Abgerundeter Bauch aufgrund von Adipositas, behandelbar, nicht schmerzhaft oder druckempfindlich bei Palpation; Leber bei tiefer Inspiration am Bogen tastbar. Milz nicht tastbar. Beidseitiges Drucködem mit Fovea-Zeichen im distalen Drittel des Beins; kein Jugular-Turgor, aber Vorliegen eines hepatojugulären Refluxes.
Die bei der Aufnahme in die Abteilung durchgeführten Tests bestätigen das Vorliegen einer schweren Anämie. Die Nierenfunktion, die Elektrolyte und die Ergebnisse der Urinuntersuchung lagen innerhalb der Normwerte. Serologische Tests auf Lungenentzündung bestätigten das Vorliegen von IgA- und IgG-Antikörpern gegen Chlamydia pneumoniae, während serologische Tests auf Mycoplasma und Pneumococcus sowie das Legionella-Antigen im Urin negativ waren.
Daher wird eine Antibiotikatherapie eingeleitet, die angesichts der kürzlichen Hospitalisierung die Verwendung einer Kombination aus Levofloxacin + Piperacillin/Tazobactam umfasst. Außerdem werden eine Diuretikatherapie und eine Sauerstofftherapie verordnet. Eine Bluttransfusion wird empfohlen, die die Patientin erneut ablehnt.
Es wurden Tests durchgeführt, um andere Ursachen für die Anämie auszuschließen:
- Knochenmarkbiopsie: normale Darstellung der Zellpopulationen des Knochenmarks;
- Ösophagogastroduodenoskopie: innerhalb der Normwerte;
- Koloskopie: multiple kolorektale Polypen (die histologische Untersuchung zeigt tubuläre Adenome mit geringer Dysplasie); Polypektomien; Divertikulose des Colon transversum und Colon ascendens; hämorrhoidale Stauung.
Während des Krankenhausaufenthalts verbesserten sich die Hämoglobinwerte, aber es blieb eine signifikante Ateminsuffizienz bestehen. Darüber hinaus blieb die Hypereosinophilie bestehen und erreichte bis zu 5.000 Zellen/µl (33 % der Leukozyten).
Angesichts dieser Daten und der Tatsache, dass die Patientin kürzlich eine weitere Lungenentzündung erlitten hatte, wurde eine weitere CT-Untersuchung des Brustkorbs durchgeführt. Wie aus den Bildern ersichtlich, bestätigte die CT-Untersuchung das Vorhandensein mehrerer milchglasartiger Trübungen in der Lunge, wobei sich einige Läsionen im Vergleich zur vorherigen CT-Untersuchung verbessert und andere verschlechtert hatten.
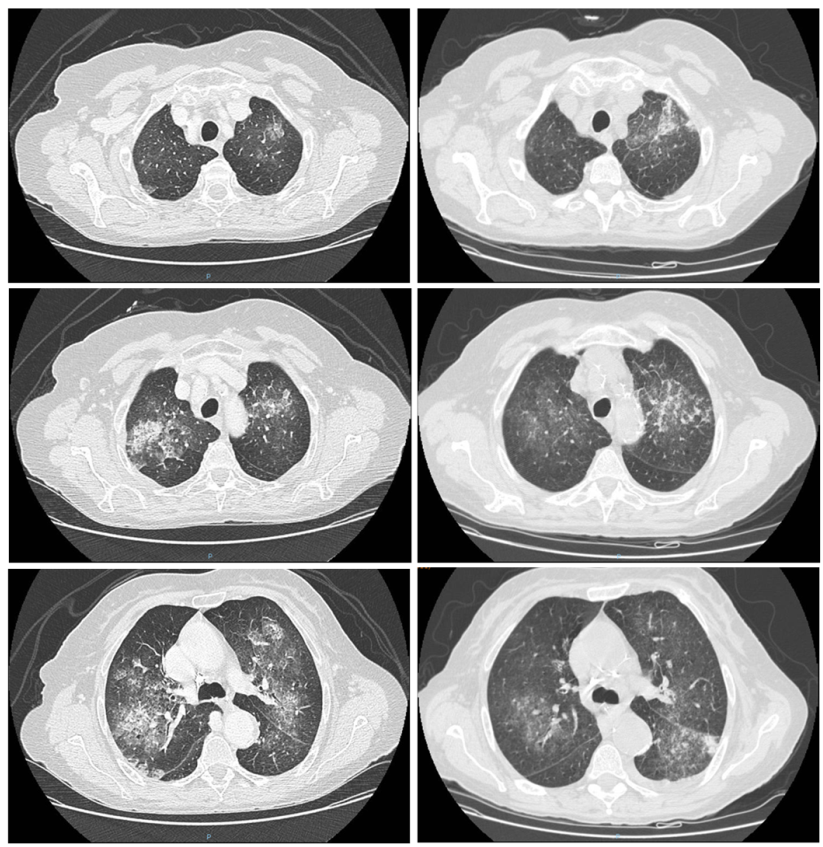
Hochauflösende CT-Aufnahme des Brustkorbs. Die Bilder auf der linken Seite beziehen sich auf die CT-Aufnahme, die einen Monat zuvor durchgeführt wurde; die Bilder auf der rechten Seite beziehen sich auf die CT-Aufnahme, die während des aktuellen Krankenhausaufenthalts durchgeführt wurde. Der Vergleich zeigt erhebliche Veränderungen der zuvor beschriebenen Trübungen, von denen sich einige verbessert haben (rechte Lunge) und andere radiologisch verschlechtert haben (Spitze und oberes Segment der linken Lunge).
Finden Sie heraus, ob Sie richtig lagen
Klinische Überlegungen zur Diagnosestellung
Das klinische Bild wirft die Frage nach der Differentialdiagnose einer Pneumonie in Verbindung mit Hypereosinophilie auf. Die wichtigsten in diesem Zusammenhang zu berücksichtigenden Ursachen sind nachstehend aufgeführt.
- Helmintheninfektionen: Die wichtigsten verantwortlichen Erreger sind Ascaris (A. lumbricoides und A. suum), Ancylostoma duodenale, Necator Americanus, Toxocara Canis, Trichinella, Schistosoma und Strongyloides Stercoralis. Unsere Patientin gibt an, in den vergangenen Jahren keine Auslandsreisen unternommen zu haben. Darüber hinaus gibt es keine Hinweise auf Kontakt mit Haus- oder Wildtieren und auch kein Risiko einer Infektion mit Strongyloides (die Patientin hat keinen Gemüsegarten und hält sich nicht regelmäßig in der freien Natur auf). Es wurde jedoch eine direkte Untersuchung auf Parasiten im Stuhl und in den Atemwegssekreten durchgeführt, die ebenso wie die Serologie auf Strongyloides Stercoralis negativ ausfiel.
- Reaktion auf Medikamente und Toxine: Das Spektrum der iatrogenen klinischen Manifestationen kann von einer asymptomatischen Verdickung bis hin zu potenziell tödlichen Erkrankungen wie DRESS (Drug Reaction with Eosinophilia and Systemic Symptoms) reichen. Diese Hypothese wird bei dieser Patientin durch ihre Medikamentenanamnese nicht gestützt, die bis auf inhalative Steroide, die sie seit Jahren einnimmt, im Wesentlichen unverändert ist.
- Akute idiopathische Pneumonie: Tritt in der Regel nach Beginn oder Wiederaufnahme des Zigarettenrauchens auf; ebenso kann sie durch akute Exposition gegenüber chemischen Stäuben und Dämpfen verursacht werden.
- Chronische eosinophile Pneumonie: Betrifft vor allem nicht rauchende Frauen, wie in diesem Fall, aber in der Regel mit einer subpleuralen Beteiligung, die sich deutlich von der bei der Patientin beobachteten unterscheidet. Es kann mit einer früheren Strahlentherapie bei Brustkrebs in Zusammenhang stehen.
- Allergische bronchopulmonale Aspergillose: Eine komplexe Überempfindlichkeitsreaktion, die durch die Exposition gegenüber Aspergillus verursacht wird. Sie manifestiert sich in der Regel hauptsächlich in Form von chronischem Asthma mit häufigen Exazerbationen. Sie geht mit Fieber, Unwohlsein, Hämoptyse und peripherer Eosinophilie einher. Auch in diesem Fall ist das CT-Bild jedoch anders, da Bronchiektasien vorherrschen, die hauptsächlich die Apikalen betreffen.
- Hypereosinophile Syndrome: Hierbei handelt es sich um paraneoplastische, reaktive oder idiopathische Syndrome, die durch das Vorliegen einer Hypereosinophilie (> 1.500 Zellen/µl) und eine mögliche Beteiligung anderer Organe (Lunge, Herz, Gehirn, Magen-Darm-Trakt, Nieren) gekennzeichnet sind. Die klinischen Manifestationen werden durch eine eosinophile Infiltration des Gewebes verursacht. Die Diagnose wird bei Vorliegen kompatibler klinischer Manifestationen und Hypereosinophilie gestellt, nachdem andere klinische Zustände, die für das Krankheitsbild verantwortlich sein könnten, ausgeschlossen wurden.
- Eosinophile Granulomatose mit Polyangiitis (EGPA, früher bekannt als Churg-Strauss-Syndrom): ANCA-assoziierte Vaskulitis, die durch das Vorliegen von Sinusitis, Asthma und peripherer Hypereosinophilie gekennzeichnet ist. Radiologisch gekennzeichnet durch vorübergehende pulmonale Opazitäten.
Angesichts des klinischen Verdachts auf eosinophile Granulomatose mit Polyangiitis wurden weitere Untersuchungen durchgeführt:
- HNO-Untersuchung: Auf der rechten Seite schienen die Schleimhaut an der Nasenscheidewand und die untere Nasenmuschel von Läsionen betroffen zu sein, die vermutlich vaskulitischen Ursprungs waren.
- P-ANCA-Test, der mit einem hohen Titer (186 IU/ml) positiv ausfiel.
Eosinophile Granulomatose mit Polyangiitis (EGPA)
Die eosinophile Granulomatose mit Polyangiitis (EGPA), früher bekannt als Churg-Strauss-Syndrom, ist eine systemische nekrotisierende Vaskulitis, die kleine und mittelgroße Blutgefäße betrifft und durch periphere Eosinophilie, Asthma, Rhinosinusitis mit oder ohne Polypen und die Beteiligung anderer Organe gekennzeichnet ist. Die EGPA wird zu den sogenannten ANCA-assoziierten systemischen Vaskulitiden (Anti-Neutrophilen-Zytoplasma-Autoantikörper) gezählt, obwohl nur 30–40 % der Patienten ANCA-positiv sind. ANCA, in der Regel der p-ANCA-Variante (Myeloperoxidase), kann dabei helfen, zwei verschiedene Untergruppen innerhalb der EGPA zu unterscheiden. ANCA-positive EGPA-Patienten zeigen häufig Symptome wie multiple Mononeuritis, halbmondförmige Glomerulonephritis und kutane Purpura. Im Gegensatz dazu weisen ANCA-negative Patienten häufiger Lungeninfiltrate, Nasenpolypen, Myokarditis und Pleuritis auf. Andere klinische Manifestationen wie systemische Symptome (Fieber, Asthenie, Arthromyalgie und Gewichtsverlust) weisen bei den beiden Subtypen der EGPA eine ähnliche Verteilung auf. Die EGPA ist eine seltene Erkrankung mit einer der niedrigsten Inzidenz- und Prävalenzraten im Vergleich zu anderen systemischen Vaskulitiden. In Europa zeigen Daten der French Vasculitis Study Group eine Prävalenz zwischen 10,7 und 13 Fällen pro Million Einwohner, mit einer Inzidenz von 0,5 bis 0,8 neuen Fällen pro Jahr pro Million Einwohner. Der Ausbruch kann zu jedem Zeitpunkt im Leben erfolgen, obwohl die Erkrankung häufiger im Erwachsenenalter auftritt, mit einem Durchschnittsalter von etwa 50 Jahren. Die Erkrankung ist bei Kindern sehr selten.
Die Ätiologie der EGPA ist nach wie vor unbekannt. Es ist daher unklar, was die eosinophile Entzündung und die unkontrollierte Aktivierung des Immunsystems mit einem Zytokinsturm verursacht.
Die Klassifizierungskriterien wurden 2022 vom American College of Rheumatology/European Alliance of Associations for Rheumatology (EULAR) überarbeitet und umfassen Folgendes:
- Asthma (+ 3 Punkte)
- Nasenpolypen (+ 3 Punkte)
- multiple Mononeuritis oder Polyneuropathie (+ 1 Punkt)
- Eosinophilie > 10 % im peripheren Blut (5 Punkte)
- histologischer Nachweis einer Vaskulitis mit extravaskulären Eosinophilen (+ 2 Punkte)
- erhöhte cANCA (zytoplasmatische antineutrophile zytoplasmatische Antikörper) oder Anti-Proteinase-3-Antikörper (minus 3 Punkte)
- Hämaturie (minus 1 Punkt)
Ein Wert von ≥ 6 hat eine Sensitivität von 85 % und eine Spezifität von 99 %.
Klinischer Verlauf und Ergebnis
Aufgrund des klinischen Bildes wurde die Diagnose EGPA gestellt. Der Patient litt unter Asthma, Hypereosinophilie, vorübergehenden und wandernden Lungeninfiltraten und einer HNO-Erkrankung (bei der Befragung gab die Patientin an, an einer chronischen Sinusitis zu leiden). Da keine negativen Prognosefaktoren vorlagen, wurde eine Steroidtherapie mit einer Dosis von 1 mg/kg/Tag Prednison begonnen, die anschließend mit Methotrexat kombiniert wurde. Ab der ersten Verabreichung von Steroiden wurde eine deutliche Verbesserung der Blutwerte beobachtet, mit einer vollständigen Reduktion der Eosinophilenzahl, die auch 3 Monate nach Beginn der Therapie weiterhin negativ blieb. Darüber hinaus wurde eine progressive Verbesserung der Atemwegsbeschwerden beobachtet, mit Rückgang der Ateminsuffizienz.
Die Patientin wurde nach 13 Tagen Krankenhausaufenthalt entlassen. Darüber hinaus wurde nach Beginn der Eisentherapie eine fortschreitende Normalisierung der Hämoglobinwerte beobachtet. Die Anämie wurde auf einen chronischen Verlust durch Darmpolypen zurückgeführt, in Verbindung mit einer wahrscheinlichen Komponente, die auf die zugrunde liegende chronische Erkrankung zurückzuführen ist.
- Bellan M, Delsignore E, Manfrinato C, Critto O, Barasolo G, Francese M, Olivetto L, Terribile R, Bertoncelli MC. Un caso di polmonite associata a ipereosinofilia. Federazione delle Associazioni dei Dirigenti Ospedalieri Internisti. 01 feb 2018
- Solans-Laqué R, Rúa-Figueroa I, Blanco Aparicio M, García Moguel I, Blanco R, Pérez Grimaldi F, Noblejas Mozo A, Labrador Horrillo M, Álvaro-Gracia JM, Domingo Ribas C, Espigol-Frigolé G, Sánchez-Toril López F, Ortiz Sanjuán FM, Arismendi E, Cid MC. Red flags for clinical suspicion of eosinophilic granulomatosis with polyangiitis (EGPA). Eur J Intern Med. 2024 Oct;128:45-52. doi: 10.1016/j.ejim.2024.06.008. Epub 2024 Jun 15. PMID: 38880725.
- Emmi G, Bettiol A, Gelain E, Bajema IM, Berti A, Burns S, Cid MC, Cohen Tervaert JW, Cottin V, Durante E, Holle JU, Mahr AD, Del Pero MM, Marvisi C, Mills J, Moiseev S, Moosig F, Mukhtyar C, Neumann T, Olivotto I, Salvarani C, Seeliger B, Sinico RA, Taillé C, Terrier B, Venhoff N, Bertsias G, Guillevin L, Jayne DRW, Vaglio A. Evidence-Based Guideline for the diagnosis and management of eosinophilic granulomatosis with polyangiitis. Nat Rev Rheumatol. 2023 Jun;19(6):378-393. doi: 10.1038/s41584-023-00958-w. Epub 2023 May 9. PMID: 37161084.
- Chung SA, Langford CA, Maz M, Abril A, Gorelik M, Guyatt G, Archer AM, Conn DL, Full KA, Grayson PC, Ibarra MF, Imundo LF, Kim S, Merkel PA, Rhee RL, Seo P, Stone JH, Sule S, Sundel RP, Vitobaldi OI, Warner A, Byram K, Dua AB, Husainat N, James KE, Kalot MA, Lin YC, Springer JM, Turgunbaev M, Villa-Forte A, Turner AS, Mustafa RA. 2021 American College of Rheumatology/Vasculitis Foundation Guideline for the Management of Antineutrophil Cytoplasmic Antibody-Associated Vasculitis. Arthritis Rheumatol. 2021 Aug;73(8):1366-1383. doi: 10.1002/art.41773. Epub 2021 Jul 8. PMID: 34235894.
- Pyo JY, Lee LE, Park YB, Lee SW. Comparison of the 2022 ACR/EULAR Classification Criteria for Antineutrophil Cytoplasmic Antibody-Associated Vasculitis with Previous Criteria. Yonsei Med J. 2023 Jan;64(1):11-17. doi: 10.3349/ymj.2022.0435. PMID: 36579374; PMCID: PMC9826961.

